题目内容
下列各组离子,能在溶液中大量共存的是( )
| A、NH4+、Cl-、SO42-、OH- |
| B、Fe2+、NO3-、Na+、OH- |
| C、Ba2+、CO32-、SO42-、Cl- |
| D、K+、NH4+、CO32-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:根据离子之间不能结合生成沉淀、气体、水、弱电解质等,则离子大量共存,以此来解答.
解答:
解:A.NH4+、OH-结合生成弱电解质,不能大量共存,故A不选;
B.Fe2+、OH-结合生成沉淀,不能共存,故B不选;
C.Ba2+分别与CO32-、SO42-结合生成沉淀,不能大量共存,故C不选;
D.该组离子之间不反应,可大量共存,故D选;
故选D.
B.Fe2+、OH-结合生成沉淀,不能共存,故B不选;
C.Ba2+分别与CO32-、SO42-结合生成沉淀,不能大量共存,故C不选;
D.该组离子之间不反应,可大量共存,故D选;
故选D.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
某无色透明溶液,在酸性环境下能大量共存的离子组是( )
| A、Na+K+AlO2-Cl- |
| B、Na+SO42-HCO3-C1- |
| C、K+MnO4- NO3-Fe2+ |
| D、Mg2+Cl-NH4+SO42- |
下列操作或叙述正确的是( )
| A、配制1mol?L-1NaOH溶液时,将溶解后的NaOH溶液立即注入容量瓶 | ||
| B、用小刀切下一小块金属钠,将剩余的钠再放回原试剂瓶 | ||
C、向某溶液中加入BaCl2溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有S
| ||
| D、向沸水中逐滴滴加1mol?L-1FeCl3溶液,并不断用玻璃棒搅拌,可制得Fe(OH)3胶体 |
下列反应,属于复分解反应的是( )
| A、CaCO3═CaO+CO2↑ |
| B、2HClO═2HCl+O2↑ |
| C、NaOH+HCl═NaCl+H2O |
| D、Fe+CuSO4═FeSO4+Cu |
大气层中的臭氧层(O3)能吸收太阳光中的紫外线,下列关于O3的分类正确的是( )
| A、化合物 | B、单质 |
| C、氧化物 | D、混合物 |
下列关于晶体与非晶体的说法不正确的是( )
| A、区别晶体与非晶体最可靠的科学方法是对固体进行x-射线衍射实验 |
| B、非晶体中粒子的排列无序,所以非晶体具有各向异性 |
| C、晶体有自范性 |
| D、非晶体无固定熔点 |
铆在铜板上的铁铆钉(如图所示),处于酸性不强的水膜中.下列有关说法正确的是( )
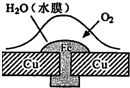

| A、铁铆钉在此环境下不易被腐蚀 |
| B、原电池反应的化学方程式:2Fe+O2+2H2O═2Fe(OH)2 |
| C、与铁接触的水膜发生反应:O2+4Fe-+2H2O═4OH- |
| D、如果在酸雨环境中,将发生:Cu-2e-═Cu2+ |
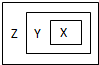 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )