题目内容
下列有关说法正确的是( )
| A、常温下,4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,则该反应的△H<0 | B、检验某物质是否含有Fe2O3的操作步骤是:样品粉碎→加水溶解→过滤,向滤液中滴加KSCN溶液 | C、锌与稀硫酸反应时加少量硫酸铜,反应加快的主要原因是Cu2+水解增大了H+浓度 | D、常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,则常温下Ksp (BaCO3)<Ksp (BaSO4) |
分析:A、根据△G=△H-T?△S判断;
B、Fe2O3难溶于水,应该用盐酸溶解;
C、形成原电池能加快反应速率;
D、洗净的沉淀中加稀盐酸,有气泡产生,不一定能说明Ksp(BaCO3)<Ksp(BaSO4),能否形成沉淀与溶液中的离子浓度有关.
B、Fe2O3难溶于水,应该用盐酸溶解;
C、形成原电池能加快反应速率;
D、洗净的沉淀中加稀盐酸,有气泡产生,不一定能说明Ksp(BaCO3)<Ksp(BaSO4),能否形成沉淀与溶液中的离子浓度有关.
解答:解:A、△G=△H-T?△S<0,反应自发进行,常温下,4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,已知该反应的气体的物质的量减少,则△S>0,所以反应的△H<0,故A正确;
B、Fe2O3难溶于水,应该用盐酸溶解,所以检验某物质是否含有Fe2O3的操作步骤是:样品粉碎→加盐酸溶解→过滤,向滤液中滴加KSCN溶液;故B错误;
C、锌与稀硫酸反应时加少量硫酸铜,Cu、Zn及稀硫酸能形成原电池,原电池能加快反应速率,故C错误;
D、洗净的沉淀中加稀盐酸,有气泡产生,不一定能说明Ksp(BaCO3)<Ksp(BaSO4),能否形成沉淀与溶液中的离子浓度有关,
当c(Ba2+)×c(CO32-)>Ksp(BaCO3)就能析出沉淀,故D错误.
故选A.
B、Fe2O3难溶于水,应该用盐酸溶解,所以检验某物质是否含有Fe2O3的操作步骤是:样品粉碎→加盐酸溶解→过滤,向滤液中滴加KSCN溶液;故B错误;
C、锌与稀硫酸反应时加少量硫酸铜,Cu、Zn及稀硫酸能形成原电池,原电池能加快反应速率,故C错误;
D、洗净的沉淀中加稀盐酸,有气泡产生,不一定能说明Ksp(BaCO3)<Ksp(BaSO4),能否形成沉淀与溶液中的离子浓度有关,
当c(Ba2+)×c(CO32-)>Ksp(BaCO3)就能析出沉淀,故D错误.
故选A.
点评:本题考查了反应的自发性判断,物质的检验,原电池原理的应用,沉淀的转化;属于基本原理的应用的考查,本题难度不大,注意基础知识的积累.

练习册系列答案
相关题目
 (2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )
(2012?绵阳模拟)钾在氧气中燃烧时得到一种钾的氧化物晶体,其结构如图所示,下列有关说法正确的是( )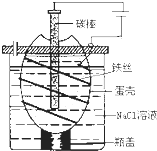 工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,
工业上通过电解饱和氯化钠溶液的方法获得氢氧化钠和氯气,图为某实验小组自制的电解饱和食盐水的简易装置,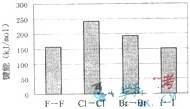 (2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(2009?上海)海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.