题目内容
常温下,在溶液中可发生以下反应:①2Fe2++Br2=2Fe3++2Br- ②2Br-+Cl2=Br2+2Cl- ③2Fe3++2I-=2Fe2++I2.由此判断下列说法正确的是( )
| A、铁元素在反应①中被还原,在③中被氧化 |
| B、反应②中当有1mol Cl2被氧化时,有2mol Br-被还原 |
| C、氧化性强弱顺序为:Cl2>I2>Br2>Fe3+ |
| D、还原性强弱顺序为:I->Fe2+>Br->Cl- |
考点:氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:A.根据化合价变化进行判断;
B.根据化合价变化及方程式进行判断;
C.氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.氧化还原反应中,还原剂的还原性大于还原产物的还原性.
B.根据化合价变化及方程式进行判断;
C.氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.氧化还原反应中,还原剂的还原性大于还原产物的还原性.
解答:
解:A.在2Fe2++Br2=2Fe3++2Br-中,铁的化合价升高,被氧化;在2Fe3++2I-=2Fe2++I2中,铁的化合价降低,被还原,故A错误;
B.在2Br-+Cl2=Br2+2Cl-中,氯元素的化合价降低,被还原,溴元素的化合价升高,被氧化,故有1molCl2被还原时,则有2molBr-被氧化,故B错误;
C.氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,在反应2Fe2++Br2=2Fe3++2Br-中,氧化剂是Br2,氧化产物是Fe3+,所以氧化性Br2>Fe3+,在反应2Br-+Cl2=Br2+2Cl-中,氧化剂是Cl2,氧化产物是Br2,所以氧化性Cl2>Br2,在反应2Fe3++2I-=2Fe2++I2中,氧化剂是Fe3+,氧化产物是I2,所以氧化性Fe3+>I2,故氧化性顺序是:Cl2>Br2>Fe3+>I2,故C错误;
D.氧化还原反应中,还原剂的还原性大于还原产物的还原性,在反应2Fe2++Br2=2Fe3++2Br-中,还原剂是Fe2+,还原产物是Br-,所以还原性Fe2+>Br-,在反应2Br-+Cl2=Br2+2Cl-中,还原剂是Br-,还原产物是Cl-,所以还原性Br->Cl-,在反应2Fe3++2I-=2Fe2++I2中,还原剂是I-,还原产物是Fe2+,所以还原性I->Fe2+,故还原性顺序是:I->Fe2+>Br->Cl-,故D正确,
故选D.
B.在2Br-+Cl2=Br2+2Cl-中,氯元素的化合价降低,被还原,溴元素的化合价升高,被氧化,故有1molCl2被还原时,则有2molBr-被氧化,故B错误;
C.氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,在反应2Fe2++Br2=2Fe3++2Br-中,氧化剂是Br2,氧化产物是Fe3+,所以氧化性Br2>Fe3+,在反应2Br-+Cl2=Br2+2Cl-中,氧化剂是Cl2,氧化产物是Br2,所以氧化性Cl2>Br2,在反应2Fe3++2I-=2Fe2++I2中,氧化剂是Fe3+,氧化产物是I2,所以氧化性Fe3+>I2,故氧化性顺序是:Cl2>Br2>Fe3+>I2,故C错误;
D.氧化还原反应中,还原剂的还原性大于还原产物的还原性,在反应2Fe2++Br2=2Fe3++2Br-中,还原剂是Fe2+,还原产物是Br-,所以还原性Fe2+>Br-,在反应2Br-+Cl2=Br2+2Cl-中,还原剂是Br-,还原产物是Cl-,所以还原性Br->Cl-,在反应2Fe3++2I-=2Fe2++I2中,还原剂是I-,还原产物是Fe2+,所以还原性I->Fe2+,故还原性顺序是:I->Fe2+>Br->Cl-,故D正确,
故选D.
点评:本题考查学生氧化还原反应中氧化性和还原性强弱判断规律:氧化还原反应中还原剂的还原性强于还原产物的还原性,氧化剂的氧化性强于氧化产物的氧化性.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
在室温下,100ml 0.1mol/L的醋酸溶液中,欲使其溶液的pH值减小,但又要使醋酸电离程度减少,应采取( )
| A、加入少量CH3COONa固体 |
| B、通入少量氯化氢气体 |
| C、提高温度 |
| D、加入少量纯醋酸 |
下列各组离子,在水溶液中能大量共存的是( )
(1)K+ Fe2+ SO42- ClO- (2)K+ Al3+ Cl- CO32-
(3)ClO- Cl- K+ OH-(4)Fe3+ Cu2+ SO42- Cl-
(5)Na+ K+ AlO2- HCO3- (6)H+ Fe2+ SO42- NO3-.
(1)K+ Fe2+ SO42- ClO- (2)K+ Al3+ Cl- CO32-
(3)ClO- Cl- K+ OH-(4)Fe3+ Cu2+ SO42- Cl-
(5)Na+ K+ AlO2- HCO3- (6)H+ Fe2+ SO42- NO3-.
| A、(1)和(6) |
| B、(3)和(4) |
| C、(1)和(4) |
| D、(2)和(5) |
下列变化可用同一原理解释的是( )
| A、氯水和SO2可使品红褪色 |
| B、氯水和活性炭使红墨水褪色 |
| C、浓硫酸和浓盐酸长期暴露在空气中浓度降低 |
| D、氢氧化钠溶液和石灰水暴露在空气中变质 |
下列化学用语书写不正确的是( )
A、甲烷的电子式: | ||
B、氟化钠的电子式: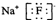 | ||
| C、硫离子的电子式:S2- | ||
D、碳-12原子:
|
下列有关实验原理、方法和结论都正确的是( )
| A、已知Cu2O+2H+═Cu2++Cu+H2O,氢气还原氧化铜后所得红色固体能完全溶于稀硫酸,说明红色固体是铜 |
| B、用蒸馏水、酚酞、BaCl2溶液和已知浓度盐酸标准溶液作试剂,可测定NaOH固体(杂质仅为Na2CO3)的纯度 |
| C、取一定量水垢加盐酸,生成能使澄清石灰水变浑浊的气体,说明水垢的主要成分为CaCO3、MgCO3 |
| D、用饱和碳酸钠溶液多次洗涤BaCO3,可除去BaCO3中少量的BaSO4,说明Ksp(BaCO3)<Ksp(BaSO4) |
有W、X、Y、Z四种物质,其中两种为单质,两种为化合物,且能发生反应:W+X→Y+Z,则Z不可能是( )
| A、F2 |
| B、Si |
| C、MgO |
| D、Al2O3 |
下列微粒中,其核外电子数相同( )
①13Al3+② ③
③ ④F-.
④F-.
①13Al3+②
 ③
③ ④F-.
④F-.| A、①②③ | B、②③④ |
| C、①②④ | D、①③④ |