题目内容
15.下列水解离子方程式正确的是( )①Na2CO3:CO${\;}_{3}^{2-}$+2H2O?H2CO3+2OH-
②NH4Cl:NH${\;}_{4}^{+}$+H2O?NH3•H2O+OH-
③NaF:F-+H2O═HF+OH-
④CuSO4:Cu2++2H2O?Cu(OH)2+2H+
⑤NaHCO3:HCO${\;}_{3}^{-}$+H2O?H3O++CO${\;}_{3}^{2-}$
⑥Na2SO3:SO${\;}_{3}^{2-}$+H2O?HSO${\;}_{3}^{-}$+OH-.
| A. | ①②③ | B. | ④⑤⑥ | C. | ④⑥ | D. | ②④⑥ |
分析 ①碳酸根离子为多元弱酸根离子,分步水解,以第一步为主;
②铵根离子水解生成一水合氨和氢离子;
③水解可逆过程,应使用可逆号;
④铜离子水解生成氢氧化铜和氢离子;
⑤碳酸氢根离子水解生成碳酸和氢氧根离子;
⑥亚硫酸根离子水解生成亚硫酸氢根离子和氢氧根离子.
解答 解:①碳酸根离子为多元弱酸根离子,分步水解,以第一步为主,水解方程式:CO32-+H2O?$\stackrel{.}{?}$HCO3-+OH-
,故错误;
②铵根离子水解生成一水合氨和氢离子,水解的离子方程式:NH4++H2O$\stackrel{.}{?}$?NH3•H2O+H+,故错误;
③氟化钠中氟离子水解生成氢氟酸和氢氧根离子,离子方程式:F-+H2O$\stackrel{.}{?}$HF+OH-,故错误;
④铜离子水解生成氢氧化铜和氢离子,离子方程式:Cu2++2H2O$\stackrel{.}{?}$?Cu(OH)2+2H+,故正确;
⑤碳酸氢根离子水解生成碳酸和氢氧根离子,离子方程式:HCO3-+H2O?$\stackrel{.}{?}$OH-+H2CO3,故错误;
⑥亚硫酸根离子水解生成亚硫酸氢根离子和氢氧根离子,离子方程式:SO32-+H2O?HSO3-+OH-,故正确;
故选:C.
点评 本题考查了盐类水解的离子方程式,明确盐类水解的规律是解题关键,注意单离子水解为可逆过程,应使用可逆符号,题目难度不大.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
6.用惰性电极电解某无色溶液时,有如下实验现象:阳极上有无色气体产生;阴极附近有白色沉淀生成.则原溶液中可能大量共存的离子组是( )
| A. | Na+、Ba2+、NO3-、Cl- | B. | H+、Mg2+、Na+、SO42- | ||
| C. | CO32-、K+、Cl-、Na+ | D. | Fe2+、NO3-、SO42-、Na+ |
10.把镁带投入盛有盐酸的敞口容器里,在下列因素中:①盐酸的浓度,②镁带的表面积,③溶液的温度,④氯离子的浓度 ⑤滴加硫酸铜溶液.对反应速率有影响的是( )
| A. | ①② | B. | ③④ | C. | ①②③④ | D. | ①②③⑤ |
20.蓄电池放电时是起原电池的作用,在充电时起电解池的作用.下式是爱迪生蓄电池分别在充电、放电时的反应:Fe+NiO2+2H2O$?_{充电}^{放电}$Fe(OH)2+Ni(OH)2下列各种推断中正确的是( )
| A. | 充电时铁做负极,NiO2做正极 | |
| B. | 放电时阴极上的电极反应为:Fe(OH)2+2e-=Fe+2OH- | |
| C. | 放电时,电解质溶液中的阴离子是向正极方向移动 | |
| D. | 蓄电池的两个电极必须浸入在碱性溶液中 |
7.下列分离混合物的操作中,一定不须加热的是( )
| A. | 过滤 | B. | 升华 | C. | 结晶 | D. | 蒸馏 |
4.某有机物的结构简式如图所示,下列有关说法中不正确的是( )


| A. | 分子式为C26H28O6N | |
| B. | 遇FeCl3溶液不能发生显色反应 | |
| C. | 1mol该物质最多能与8mol氢气发生加成反应 | |
| D. | 1mol该物质最多能与4molNaOH溶液完全反应 |
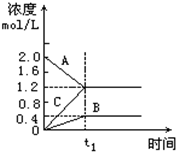 如图表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间,t1为2分钟.试回答:
如图表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间,t1为2分钟.试回答: