题目内容
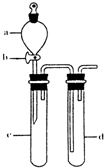
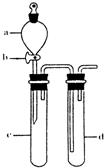
用如图所示装置可以完成一系列实验(图中夹持装置已略去)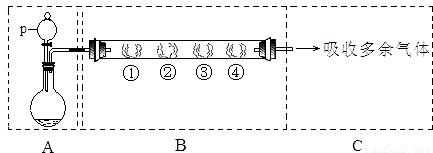
请回答下列问题:
Ⅰ.(1)仪器p的名称是______,若用装置A由浓硫酸和亚硫酸钠固体制取SO2气体,并通过装置B完成表中设计实验,请填写表中空白:
| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 淀粉和碘水混合液 | 氢硫酸 |
| 现象 | ______ | ______ | 褪色 | 浅黄色 |
| 体现SO2的性质 | 水溶液显酸性 | 漂白性 | ______ | 氧化性 |
Ⅱ.若用装置A由浓硫酸和浓盐酸混合制取HCl气体,装置B中的四处棉花依次做了如下处理:①包有某固体物质、②蘸有KI溶液、③蘸有石蕊溶液、④蘸有浓NaOH溶液.
(1)仪器p中盛装试剂的化学式为______.
(2)反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式:______.
①处包有的某固体物质可能是(填序号)______.
a.MnO2 b.KMnO4 c.KCl d.Cu
(3)在实验过程中,在③处能观察到______.
(4)反应较长时间后,②处有棕黄色褪去,生成无色的IO-3,写出该反应的离子方程式:______.
【答案】分析:Ⅰ.(1)仪器p的名称是分液漏斗;根据SO2可溶于水生成亚硫酸(H2SO3),H2SO3显酸性;根据SO2具有漂白性,能使品红溶液褪色;
根据碘能使淀粉溶液变蓝,SO2具有还原性,能与碘水反应,使蓝色退去;SO2具有氧化性,能与氢硫酸反应;
(2)SO2与碘水反应为:I2+SO2+2H2O═4H++SO2-4+2I-
II.(1)根据浓硫酸稀释的方法将浓硫酸往水中倒;
(2)先根据有棕黄色物质确定为单质碘,再根据卤素单质间能发生置换反应;由通过①后生成了Cl2,再根据KMnO4溶液能氧化HCl得到Cl2;
(3)根据Cl2能与水反应生成HCl和HClO,HCl具有酸性和HClO具有强氧化性;
(4)根据实验现象和氧化还原反应中化合价升降总数相等来解答.
解答:解:Ⅰ.(1)仪器p的名称是分液漏斗;根据SO2可溶于水生成亚硫酸(H2SO3),H2SO3显酸性;根据SO2具有漂白性,能使品红溶液褪色;
根据碘能使淀粉溶液变蓝,SO2具有还原性,能与碘水反应,使蓝色退去;SO2具有氧化性,能与氢硫酸反应;
故答案为:(1)分液漏斗;
(2)SO2与碘水反应为:SO2+I2+2H2O=H2SO4+2HI,溶液蓝色褪去,故答案为:I2+SO2+2H2O═4H++SO2-4+2I-;
II.(1)因浓硫酸和浓盐酸混合时,为了使热量散发,应将浓硫酸缓慢加入到浓盐酸中,故答案为:浓硫酸;
(2)有棕黄色物质确定为单质碘,卤素单质间能发生置换反应:Cl2+2KI=2KCl+I2,因通过①后生成了Cl2,而KMnO4溶液能氧化HCl得到Cl2,所以某固体物质可能是KMnO4,故答案为:Cl2+2I-=2Cl-+I2;b;
(3)因Cl2能与水反应生成HCl和HClO,HCl具有酸性,能使石蕊溶液变红,HClO具有强氧化性能使红色褪去,故答案为:先由紫色变红色后褪色;
(4)②处有棕黄色褪去,生成无色的IO3-,碘的化合价升高,则氯元素和化合价降低为-1价,化学方程式为:
5Cl2+I2+6H2O=2HIO3+10HCl,离子方程式为:5Cl2+I2+6H2O=12H++2IO3-+10Cl-,
故答案为:5Cl2+I2+6H2O=12H++2IO3-+10Cl-.
点评:本题主要结合实验考查了几种物质的性质,要求学生能够根据实验现象判断物质的性质.
根据碘能使淀粉溶液变蓝,SO2具有还原性,能与碘水反应,使蓝色退去;SO2具有氧化性,能与氢硫酸反应;
(2)SO2与碘水反应为:I2+SO2+2H2O═4H++SO2-4+2I-
II.(1)根据浓硫酸稀释的方法将浓硫酸往水中倒;
(2)先根据有棕黄色物质确定为单质碘,再根据卤素单质间能发生置换反应;由通过①后生成了Cl2,再根据KMnO4溶液能氧化HCl得到Cl2;
(3)根据Cl2能与水反应生成HCl和HClO,HCl具有酸性和HClO具有强氧化性;
(4)根据实验现象和氧化还原反应中化合价升降总数相等来解答.
解答:解:Ⅰ.(1)仪器p的名称是分液漏斗;根据SO2可溶于水生成亚硫酸(H2SO3),H2SO3显酸性;根据SO2具有漂白性,能使品红溶液褪色;
根据碘能使淀粉溶液变蓝,SO2具有还原性,能与碘水反应,使蓝色退去;SO2具有氧化性,能与氢硫酸反应;
故答案为:(1)分液漏斗;
| 变红 | 褪色 | |||
| 还原性 |
II.(1)因浓硫酸和浓盐酸混合时,为了使热量散发,应将浓硫酸缓慢加入到浓盐酸中,故答案为:浓硫酸;
(2)有棕黄色物质确定为单质碘,卤素单质间能发生置换反应:Cl2+2KI=2KCl+I2,因通过①后生成了Cl2,而KMnO4溶液能氧化HCl得到Cl2,所以某固体物质可能是KMnO4,故答案为:Cl2+2I-=2Cl-+I2;b;
(3)因Cl2能与水反应生成HCl和HClO,HCl具有酸性,能使石蕊溶液变红,HClO具有强氧化性能使红色褪去,故答案为:先由紫色变红色后褪色;
(4)②处有棕黄色褪去,生成无色的IO3-,碘的化合价升高,则氯元素和化合价降低为-1价,化学方程式为:
5Cl2+I2+6H2O=2HIO3+10HCl,离子方程式为:5Cl2+I2+6H2O=12H++2IO3-+10Cl-,
故答案为:5Cl2+I2+6H2O=12H++2IO3-+10Cl-.
点评:本题主要结合实验考查了几种物质的性质,要求学生能够根据实验现象判断物质的性质.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
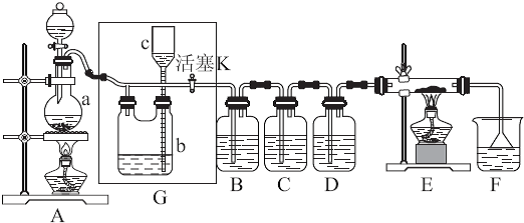
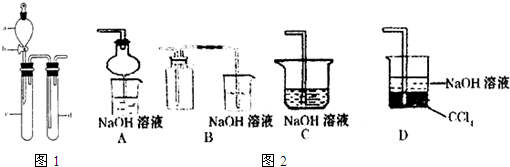
 SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.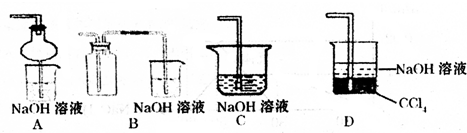
 SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.