题目内容
下列说法正确的是( )
| A、向含有1 mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总的物质的量为2mol |
| B、裂解、煤的汽化、石油减压分馏、甲苯制TNT等过程中都包含化学变化 |
| C、需要通电才可进行的有:电离、电解、电镀、电化学腐蚀 |
| D、乙醇和乙烯的物质的量均为1mol,完成燃烧消耗的氧气的质量相同 |
考点:石油的分馏产品和用途,化学方程式的有关计算,原电池和电解池的工作原理,电解质在水溶液中的电离,有机物实验式和分子式的确定,石油的裂化和裂解,煤的干馏和综合利用
专题:
分析:A.1mol KAl(SO4)2含有1molAl3+,2molSO42-,开始发生反应SO42-+Ba2+=BaSO4↓,Al3++3OH-=A1(OH)3↓,Al3+完全沉淀,再继续滴加Ba(OH)2溶液,发生反应A1(OH)3+OH-=A1O2-+2H2O,SO42-+Ba2+=BaSO4↓,判断Al3+完全沉淀后再滴加Ba(OH)2溶液沉淀量的物质的量变化,确定沉淀量最大时发生的反应,注意此时钡离子与氢氧根离子为1:2;
B.有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化;
C.电离是电解质在水溶液中离解出自由移动离子的过程;
电解池是外加电源强迫下的氧化还原反应;
电镀池实质是一个电解池;
电化学腐蚀原理是原电池原理;
D.设有机物的化学式为CxHyOz,1mol该有机物消耗的氧气的物质的量为(x+
-
),分别计算每种有机物充分燃烧的耗氧量,然后进行比较.
B.有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化;
C.电离是电解质在水溶液中离解出自由移动离子的过程;
电解池是外加电源强迫下的氧化还原反应;
电镀池实质是一个电解池;
电化学腐蚀原理是原电池原理;
D.设有机物的化学式为CxHyOz,1mol该有机物消耗的氧气的物质的量为(x+
| y |
| 4 |
| z |
| 2 |
解答:
解:A.1mol KAl(SO4)2含有1molAl3+、2molSO42-,
开始发生反应SO42-+Ba2+=BaSO4↓,Al3++3OH-=A1(OH)3↓,
由方程式可知当加入1.5molBa(OH)2时,Al3+完全沉淀,SO42-反应1.5mol,SO42-有剩余,再继续滴加Ba(OH)2溶液,
发生反应A1(OH)3+OH-=A1O2-+2H2O,SO42-+Ba2+=BaSO4,
由方程式可知加入1molBa(OH)2,溶解2molA1(OH)3,生成1molBaSO4,
沉淀的物质的量减少,故当Al3+恰好沉淀时,生成的沉淀的物质的量最大,此时加入1.5molBa(OH)2,
由SO42-+Ba2+=BaSO4↓可知生成硫酸钡沉淀1.5mol,由Al3++3OH-=A1(OH)3↓可知生成氢氧化铝沉淀1mol,
故沉淀物质的量最大为1.5mol+1mol=2.5mol,故A错误;
B.石油减压分馏没有新物质生成,是物理变化,故B错误;
C.电离是电解质在水溶液中离解出自由移动离子的过程,不需要通电;电解池是外加电源强迫下的氧化还原反应,必须加外加电源;电镀池实质是一个电解池,必须加外加电源;电化学腐蚀原理是原电池原理,原电池中不含电源,故C错误;
D.乙醇和乙烯的物质的量均为1mol,耗氧量为3mol,故D错误.
故选D.
开始发生反应SO42-+Ba2+=BaSO4↓,Al3++3OH-=A1(OH)3↓,
由方程式可知当加入1.5molBa(OH)2时,Al3+完全沉淀,SO42-反应1.5mol,SO42-有剩余,再继续滴加Ba(OH)2溶液,
发生反应A1(OH)3+OH-=A1O2-+2H2O,SO42-+Ba2+=BaSO4,
由方程式可知加入1molBa(OH)2,溶解2molA1(OH)3,生成1molBaSO4,
沉淀的物质的量减少,故当Al3+恰好沉淀时,生成的沉淀的物质的量最大,此时加入1.5molBa(OH)2,
由SO42-+Ba2+=BaSO4↓可知生成硫酸钡沉淀1.5mol,由Al3++3OH-=A1(OH)3↓可知生成氢氧化铝沉淀1mol,
故沉淀物质的量最大为1.5mol+1mol=2.5mol,故A错误;
B.石油减压分馏没有新物质生成,是物理变化,故B错误;
C.电离是电解质在水溶液中离解出自由移动离子的过程,不需要通电;电解池是外加电源强迫下的氧化还原反应,必须加外加电源;电镀池实质是一个电解池,必须加外加电源;电化学腐蚀原理是原电池原理,原电池中不含电源,故C错误;
D.乙醇和乙烯的物质的量均为1mol,耗氧量为3mol,故D错误.
故选D.
点评:本题考查化学方程式的计算、化学变化和有机物耗氧量的计算等,题目难度不大,注意把握有机物与氧气反应的化学方程式的书写.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、热的纯碱液去油污效果好,因为加热可使CO32-的水解程度增大,溶液碱性增强,去污力增强 | ||||
| B、铁在潮湿的环境下生锈以及Mg与NH4Cl溶液反应生成H2都与盐类水解有关 | ||||
| C、将Al2(SO4)3溶液加热、蒸干、灼烧,可得到固体Al2(SO4)3 | ||||
D、将饱和FeCl3溶液滴入沸水中制胶体,离子方程式:Fe3++3H2O
|
下列化学用语的书写,不正确的是( )
| A、葡萄糖的分子式:C6H12O6 |
| B、氯气的电子式:Cl:Cl |
| C、乙醇的结构简式:CH3CH2OH |
D、硫原子的结构示意图: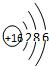 |
下列关于仪器的识别中错误的是( )
A、 分液漏斗 |
B、 蒸发皿 |
C、 坩埚钳 |
D、 滴瓶 |
足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与3.36LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入2.5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A、60mL | B、240mL |
| C、30mL | D、120mL |
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A、在常温常压下,11.2 L N2含有的分子数为NA |
| B、标准状况下,18 g H2O所占的体积约是22.4 L |
| C、32 g O2在标准状况下所占的体积约为22.4 L |
| D、1 mol Ne中约含有6.02×1024个电子 |
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )


| A、属于芳香烃 |
| B、属于卤代烃 |
| C、该有机物有四种官能团 |
| D、该有机物的分子式为C23H21O3NBr2 |
在实验室中,欲从碘水中提取出碘,最好采用的方法是( )
| A、过滤 | B、蒸发 | C、萃取 | D、蒸馏 |
 已知A、B、C、D、E五种物质,且A、B、C、D的焰色反应均为黄色,它们的关系如图所示,已知E为气体单质,能使带火星的木条复燃.
已知A、B、C、D、E五种物质,且A、B、C、D的焰色反应均为黄色,它们的关系如图所示,已知E为气体单质,能使带火星的木条复燃.