题目内容
足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与3.36LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入2.5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A、60mL | B、240mL |
| C、30mL | D、120mL |
考点:化学方程式的有关计算
专题:计算题
分析:足量的Cu与一定量的浓HNO3反应得到硝酸铜溶液和NO2、N2O4、NO的混合气体,混合气体与3.36L O2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸,则Cu提供的电子物质的量等于氧气获得电子的物质的量,据此计算Cu2+的物质的量,进而计算Cu2+恰好完全沉淀需要氢氧化钠的物质的量,再根据V=
计算氢氧化钠溶液的体积.
| n |
| c |
解答:
解:3.36L O2的物质的量为
=0.15mol,NO2、N2O4、NO的混合气体与3.36L O2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成硝酸,根据电子转移守恒,Cu提供的电子物质的量等于氧气获得电子的物质的量,故Cu2+的物质的量=
=0.3mol,Cu2+恰好与氢氧根离子恰好反应生成Cu(OH)2,故n(NaOH)=2n(Cu2+)=0.3mol×2=0.6mol,故需要氢氧化钠溶液的体积为
=0.24L=240mL,
故选B.
| 3.36L |
| 22.4L/mol |
| 0.15mol×4 |
| 2 |
| 0.6mol |
| 2.5mol/L |
故选B.
点评:本题考查混合物的计算、氧化还原反应计算,难度中等,利用电子转移守恒,确定氧气获得的电子等于金属提供的电子是解题的关键,注意体会守恒思想的运用.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
下列体系加压后,对化学反应速率没有明显影响的是( )
| A、2SO2+O2?2SO3 |
| B、I2(g)+H2?2HI |
| C、CO2+H2O=H2CO3 |
| D、H++OH-=H2O |
某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如图甲所示t0-t1阶段c(B)未画出].图乙为t2后改变互不相同的某一条件时反应速率跟时间的关系,其中t3-t4阶段使用催化剂.下列说法正确的是( )
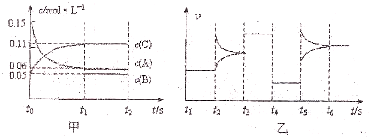

| A、若t1=15s,生成物C在t0-t1时间段的平均反应速率为0.004 mol?L-1?S-1 |
| B、t4-t5阶段改变的条件为降低反应温度 |
| C、B的起始物质的量为0.02 mol |
| D、t5-t6阶段改变的条件是增大反应物浓度 |
探究性实验:用称量法测定铁在氧气中燃烧的产物.发现5.6g铁在充足的氧气中燃烧得到7.82g固体.小芳排除其他因素可能产生的误差,则实验中得到的固体产物可能是( )
| A、Fe3O4和Fe的混合物 |
| B、Fe3O4和FeO的混合物 |
| C、Fe3O4和Fe2O3的混合物 |
| D、Fe3O4、FeO和Fe的混合物 |
下列各组物质中,只用NaOH溶液不能完成除去杂质(括号中是杂质)是( )
| A、Fe(OH)3[Al(OH)3] |
| B、MgCl2(AlCl3) |
| C、Fe(Al) |
| D、MgO(Al2O3) |
下列说法正确的是( )
| A、向含有1 mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总的物质的量为2mol |
| B、裂解、煤的汽化、石油减压分馏、甲苯制TNT等过程中都包含化学变化 |
| C、需要通电才可进行的有:电离、电解、电镀、电化学腐蚀 |
| D、乙醇和乙烯的物质的量均为1mol,完成燃烧消耗的氧气的质量相同 |
化学与生活息息相关,下列说法不正确的是( )
| A、鱼、肉、鸡蛋等富含蛋白质的食品被称为碱性食品,长期缺乏可使尿液偏酸性 |
| B、维生素C在水溶液中或受热时容易被氧化,生吃新鲜蔬菜可以减少维生素C的损失 |
| C、血红蛋白与CO结合生成碳氧血红蛋白,强于结合O2的能力,CO可使人缺氧中毒 |
| D、水中的无机汞在微生物作用下会转化成毒性更大的有机汞,日本的水俣病就是有机汞引起的汞中毒事件 |
分类是生活、学习和科学研究中常用的一种方法下列物质的分类正确的是( )
| A、NaOH、Na2CO3都属于碱 |
| B、HNO3、HClO都属于酸 |
| C、SO2、CO都属于酸性氧化物 |
| D、H2SO4、SO3都属于电解质 |
