题目内容
1.1-乙氧基萘是一种无色液体,密度比水大,不溶于水,易溶于醇、醚,熔点5.5℃,沸点267.4℃.1-乙氧基萘常用作香料,也可作为合成其他香料的原料.实验室制备1-乙氧基萘的过程如下:
(1)将72g 1-萘酚溶于100mL无水乙醇中,加入5mL浓硫酸混合.将混合液置于如图所示的容器中加热充分反应.实验中使用过量乙醇的原因是提高1-萘酚的转化率.烧瓶上连接长直玻璃管的主要作用是冷凝、回流,提高原料的利用率.
(2)反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层.为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥.正确的顺序是A(填字母代号).
A.③②④①B.①②③④C.②①③④
(3)蒸馏时所用的玻璃仪器除了酒精灯、冷凝管、接收器、锥形瓶外还有温度计、蒸馏烧瓶.
(4)实验测得1-乙氧基萘的产量与反应时间、温度的变化如图所示,时间延长、温度升高1-乙氧基萘的产量下降的原因可能是1-萘酚被氧化、温度高乙醇大量挥发或温度高发生副反应.
(5)用金属钠可检验1-乙氧基萘是否纯净,简述实验现象与加入金属钠有气泡生成则产物不纯,无气泡生成则产物纯净.
分析 (1)依据化学反应的方向分析,加入乙醇过量会提高高1-萘酚的转化率;长玻璃管起到冷凝回流的作用,提高乙醇原料的利用率;
(2)提纯产物用10%的NaOH溶液碱洗并分液,把硫酸洗涤去,水洗并分液洗去氢氧化钠,用无水氯化钙干燥并过滤,吸收水,控制沸点通过蒸馏的方法得到;
(3)依据蒸馏装置分析选择仪器;
(4)时间延长、温度升高,1-乙氧基萘的产量下降的原因可能是酚羟基被氧化,乙醇溶解等;
(5)用金属钠检验1-乙氧基萘是否纯净,依据钠和酚羟基反应生成氢气分析判断.
解答 解:(1)将72g1-萘酚溶于100mL无水乙醇中,加入5mL浓硫酸混合,将混合液置于如图1所示的容器中加热充分反应.实验中使用过量乙醇的原因是提高1-萘酚的转化率或作溶剂;乙醇易挥发,烧瓶上连接长直玻璃管的主要作用是冷凝回流,提高原料乙醇的利用率,
故答案为:提高1-萘酚的转化率;冷凝回流,提高原料乙醇的利用率;
(2)提纯产物用10%的NaOH溶液碱洗并分液,把硫酸洗涤去,水洗并分液洗去氢氧化钠,用无水氯化钙干燥并过滤,吸收水,控制沸点通过蒸馏的方法得到,实验的操作顺序为:③②④①;
故答案为:A;
(3)蒸馏装置所用的玻璃仪器除了酒精灯、冷凝管、接收器、锥形瓶外还有温度计、蒸馏烧瓶,
故答案为:温度计、蒸馏烧瓶;
(4)图象分析可知,时间延长、温度升高,1-乙氧基萘的产量下降的原因可能是酚羟基被氧化,乙醇易挥发易溶解,易发生副反应导致产量减小,
故答案为:1-萘酚被氧化;温度高乙醇大量挥发或温度高发生副反应;
(5)用金属钠检验1-乙氧基萘是否纯净,钠和酚羟基反应生成氢气,取少量经提纯的产品于试管A中,加入金属钠若无气泡产生,则产品纯净;若有气泡产生,则产品不纯,
故答案为:加入金属钠有气泡生成则产物不纯,无气泡生成则产物纯净.
点评 本题考查了有机物的性质类推分析判断,官能团的性质应用是解题关键,实验基本操作和物质性质的熟练掌握是解题关键,题目难度中等.

| A. | 分子间作用力无一定方向性 | B. | 占据晶格结点的微粒是原子 | ||
| C. | 化学键是共价键 | D. | 三者都是 |

试回答下列问题:
(1)步骤①反应器发生的反应中,转移电子总数为60e-;
(2)步骤②中,用硝酸而不用HI,其原因可能是HI具有还原性,能将已生成的碘酸氢钾还原;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为Cl2及Cl2与KOH反应生成的KClO,能将KIO3氧化成KIO4;
(4)实验中涉及两次过滤,在实验室进行过滤实验中,用到的玻璃仪器有漏斗、烧杯、玻璃;
(5)步骤⑧用氢氧化钾调节溶液的pH,反应的化学方程式为:KOH+KH(IO3)2=2KIO3+H2O;
(6)参照下表碘酸钾的溶解度,步骤
 得到碘酸钾晶体,你建议的方法是蒸发结晶.
得到碘酸钾晶体,你建议的方法是蒸发结晶.| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3 g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
| A. | 少量金属钠保存在煤油中 | |
| B. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| C. | 氢氧化钠溶液保存在配有玻璃塞的细口瓶中 | |
| D. | 氢氟酸保存在塑料试剂瓶中 |

 或
或 ;
;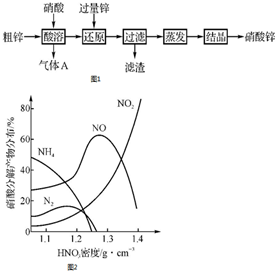 硝酸锌常用于工业电镀、媒染剂等,用粗锌[含少量Zn2(OH)2CO3、Fe和Cu]和硝酸为原料制备硝酸锌的实验流程如图1.活泼金属(如Zn、Fe、Mg等)与不同浓度HNO3溶液反应时主要还原产物不同.如图2是Fe与不同浓度HNO3溶液反应时的主要还原产物.
硝酸锌常用于工业电镀、媒染剂等,用粗锌[含少量Zn2(OH)2CO3、Fe和Cu]和硝酸为原料制备硝酸锌的实验流程如图1.活泼金属(如Zn、Fe、Mg等)与不同浓度HNO3溶液反应时主要还原产物不同.如图2是Fe与不同浓度HNO3溶液反应时的主要还原产物.
 +2H2O;
+2H2O; ;
;