题目内容
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液:
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气.
己知:Ksp[Fe(OH)3]=4.0×10-38
回答下列问题:
(1)FeCl3水解反应的离子方程式为 ;
(2)过程I 加入铁屑的主要作用是 ,分离得到固体的主要成分是 ;
(3)过程II中发生反应的化学方程式为 、 ;
(4)过程II中调节溶液的pH为5,金属离子浓度为 .
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液:
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气.
己知:Ksp[Fe(OH)3]=4.0×10-38
回答下列问题:
(1)FeCl3水解反应的离子方程式为
(2)过程I 加入铁屑的主要作用是
(3)过程II中发生反应的化学方程式为
(4)过程II中调节溶液的pH为5,金属离子浓度为
考点:铁盐和亚铁盐的相互转变,难溶电解质的溶解平衡及沉淀转化的本质,铁的化学性质
专题:元素及其化合物
分析:(1)Fe3+易水解,水解生成H+,根据水解原理书写方程式;
(2)过程Ⅰ加入铁屑的主要作用是和氯化铜发生反应生成铜,过滤后得到固体为Fe和Cu,加入盐酸铁反应,铜不反应过滤分离得到铜;
(3)滤液成分为氯化亚铁溶液,加入石灰水反应生成氢氧化亚铁沉淀,在空气中迅速氧化为氢氧化铁;
(4)过程Ⅱ中调节溶液的pH为5,氢氧化铁沉淀溶液中存在沉淀溶解平衡,依据溶度积常数计算.
(2)过程Ⅰ加入铁屑的主要作用是和氯化铜发生反应生成铜,过滤后得到固体为Fe和Cu,加入盐酸铁反应,铜不反应过滤分离得到铜;
(3)滤液成分为氯化亚铁溶液,加入石灰水反应生成氢氧化亚铁沉淀,在空气中迅速氧化为氢氧化铁;
(4)过程Ⅱ中调节溶液的pH为5,氢氧化铁沉淀溶液中存在沉淀溶解平衡,依据溶度积常数计算.
解答:
解:(1)Fe3+易水解,水解生成H+,水解的离子方程式为Fe3++3H2O?Fe(OH)3+3H+,故答案为:Fe3++3H2O?Fe(OH)3+3H+;
(2)向废液中投入过量铁屑,铁会和三氯化铁溶液反应生成氯化亚铁,和氯化铜反应生成铜和氯化亚铁,所以加入铁粉是为了得到铜,过滤得到固体是过量的铁和铜,用盐酸溶解铁反应,铜不反应过滤得到铜,
故答案为:回收铜;Cu和Fe;
(3)滤液成分为氯化亚铁溶液,加入石灰水反应生成氢氧化亚铁沉淀,在空气中迅速氧化为氢氧化铁;反应的化学方程式为:FeCl2+Ca(OH)2=Fe(OH)2↓+CaCl2、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:FeCl2+Ca(OH)2=Fe(OH)2↓+CaCl2 、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)过程Ⅱ中调节溶液的pH为5,常温下溶液中氢氧根离子浓度为10-9mol/L,依据溶度积常数计算铁离子浓度,Fe(OH)3(s)?Fe3++3OH-;Ksp=c(Fe3+)×c3(OH-),c(Fe3+)=
=4×10-11mol/L;
故答案为:4×10-11mol/L.
(2)向废液中投入过量铁屑,铁会和三氯化铁溶液反应生成氯化亚铁,和氯化铜反应生成铜和氯化亚铁,所以加入铁粉是为了得到铜,过滤得到固体是过量的铁和铜,用盐酸溶解铁反应,铜不反应过滤得到铜,
故答案为:回收铜;Cu和Fe;
(3)滤液成分为氯化亚铁溶液,加入石灰水反应生成氢氧化亚铁沉淀,在空气中迅速氧化为氢氧化铁;反应的化学方程式为:FeCl2+Ca(OH)2=Fe(OH)2↓+CaCl2、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:FeCl2+Ca(OH)2=Fe(OH)2↓+CaCl2 、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)过程Ⅱ中调节溶液的pH为5,常温下溶液中氢氧根离子浓度为10-9mol/L,依据溶度积常数计算铁离子浓度,Fe(OH)3(s)?Fe3++3OH-;Ksp=c(Fe3+)×c3(OH-),c(Fe3+)=
| 4.0×10-38 |
| (10-9)3 |
故答案为:4×10-11mol/L.
点评:本题考查了铁离子的氧化性,提取铜的反应过程和步骤分析判断,氢氧化铁氢氧化亚铁的转化反应,溶度积的计算应用,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
若(NH4)2SO4在强热时分解的产物是SO2、N2、NH3和H2O,则该反应产物中SO2和NH3的物质的量之比为( )
| A、1:4 | B、3:4 |
| C、4:1 | D、4:3 |
在标准状况下,A L NH3溶于B mL水中,得到密度为ρg/cm3的R L氨水,则此氨水的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列说法不正确的是( )
| A、在自然界中存在的单质,一定具备化学性质稳定、不与其它物质发生反应这一特征 |
| B、100多年前,英国曾耗巨资改建高炉,试图延长CO和Fe2O3的接触时间,以减少CO的排放,这违背了化学反应都有一定限度这一基本原理 |
| C、在溶液中,有色物质参与的反应,可以用分光光度计来测定其化学反应速率 |
| D、虽然碳酸钙分解需要吸收大量的热,但在高温条件下也能自发进行 |
X元素的阳离子和Y元素的阴离子具有相同的电子层结构,下列叙述正确的是( )
| A、原子序数X<Y |
| B、离子半径X<Y |
| C、原子半径X<Y |
| D、原子最外层电子数X>Y |
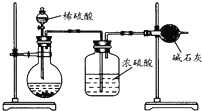 为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
为了测定氢氧化钠和碳酸钠固体混合物中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案: