题目内容
 某课外活动小组利用如图所示的装置进行乙醇的催化氧化实验制取乙醛 (试管丙中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的铜丝,约lmin后鼓入空气.请填写下列空白:
某课外活动小组利用如图所示的装置进行乙醇的催化氧化实验制取乙醛 (试管丙中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的铜丝,约lmin后鼓入空气.请填写下列空白:(1)检验乙醛的试剂是
A.银氨溶液B.碳酸氢钠溶液C.新制氢氧化铜悬浊液D.氧化铜
(2)乙醇发生催化氧化的化学反应方程式为
(3)实验时,常常将甲装置浸在70℃~80℃的水浴中,目的是
(4)该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色.该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应.请你设计一个简单的实验,探究哪一种猜想正确?
考点:性质实验方案的设计,乙醇的化学性质
专题:有机物的化学性质及推断
分析:由乙醇的催化氧化实验装置可知,气球中气体将乙醇赶入试管中,且氧气、乙醇在Cu作催化剂条件下发生反应生成乙醛,
(1)乙醛中含-CHO,可发生银镜反应、与新制氢氧化铜悬浊液生成砖红色沉淀;
(2)乙醇可以被催化氧化生成醛和水;
(3)水浴加热可以让乙醇在一定的温度下成为蒸气,从而加快反应的速率;丙中液体可倒吸进入试管中;
(4)若生成乙酸时溶液具有酸性,以此来解答.
(1)乙醛中含-CHO,可发生银镜反应、与新制氢氧化铜悬浊液生成砖红色沉淀;
(2)乙醇可以被催化氧化生成醛和水;
(3)水浴加热可以让乙醇在一定的温度下成为蒸气,从而加快反应的速率;丙中液体可倒吸进入试管中;
(4)若生成乙酸时溶液具有酸性,以此来解答.
解答:
解:由乙醇的催化氧化实验装置可知,气球中气体将乙醇赶入试管中,且氧气、乙醇在Cu作催化剂条件下发生反应生成乙醛,
(1)乙醛中含-CHO,可发生银镜反应、与新制氢氧化铜悬浊液生成砖红色沉淀,而B、D中物质与乙醛常温不反应,则检验试剂为AC,故答案为:AC;
(2)乙醇可以被催化氧化生成醛和水,反应的方程式为2CH3CH2OH+O2
2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O;
(3)将甲装置浸在70℃~80℃的水浴中,使生成乙醇蒸气的速率加快且较均匀,导气管直接插入丙溶液内,生成的乙醛和过量的乙醇易溶于水,则设计上的缺陷导致丙装置产生倒吸现象,故答案为:使生成乙醇蒸气的速率加快且较均匀;发生倒吸;
(4)若生成乙酸时溶液具有酸性,则设计实验为用pH试纸检验溴水与褪色后溶液的酸碱性,若酸性明显增强,则猜想①正确,反正猜想②正确,
故答案为:用pH试纸检验溴水与褪色后溶液的酸碱性,若酸性明显增强,则猜想①正确,反正猜想②正确.
(1)乙醛中含-CHO,可发生银镜反应、与新制氢氧化铜悬浊液生成砖红色沉淀,而B、D中物质与乙醛常温不反应,则检验试剂为AC,故答案为:AC;
(2)乙醇可以被催化氧化生成醛和水,反应的方程式为2CH3CH2OH+O2
| Cu |
| △ |
| Cu |
| △ |
(3)将甲装置浸在70℃~80℃的水浴中,使生成乙醇蒸气的速率加快且较均匀,导气管直接插入丙溶液内,生成的乙醛和过量的乙醇易溶于水,则设计上的缺陷导致丙装置产生倒吸现象,故答案为:使生成乙醇蒸气的速率加快且较均匀;发生倒吸;
(4)若生成乙酸时溶液具有酸性,则设计实验为用pH试纸检验溴水与褪色后溶液的酸碱性,若酸性明显增强,则猜想①正确,反正猜想②正确,
故答案为:用pH试纸检验溴水与褪色后溶液的酸碱性,若酸性明显增强,则猜想①正确,反正猜想②正确.
点评:本题考查性质实验方案的设计,为高频考点,把握乙醇的性质及实验装置的作用、反应原理为解答的关键,注意(4)中实验设计与产物性质有关,侧重分析与实验能力的考查,题目难度中等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
关于水在人体中的作用叙述不正确的是( )
| A、将氧气运输到血液 |
| B、将体内代谢的废物通过尿液或粪便排出体外 |
| C、营养素的消化、吸收过程不需要水的作用 |
| D、通过蒸发或出汗来调节体温保持不变 |
下列反应的离子方程式正确的是( )
| A、铁粉投醋酸溶液中:Fe+2H+=Fe2++H2↑ |
| B、Cl2溶于水:Cl2+H2O=2H++Cl-+ClO- |
| C、氢氧化钡溶液中滴加硫酸氢钠溶液至恰好为中性:Ba2++SO42-+2OH-+2H+=BaSO4↓+2H2O |
| D、向饱和澄清石灰水中加入纯碱溶液:Ca(OH)2+CO32-=CaCO3↓+2OH- |
下列实验装置或对实验现象的描述正确的是( )
A、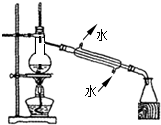 分馏装置 |
B、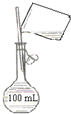 配制150 mL 0.10 mol?L-1盐酸 |
C、 烧瓶内溶液变蓝色 |
D、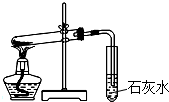 探究NaHCO3的热稳定性 |
下列各组物质互为同系物的是( )
| A、甲醇与乙醇 |
B、 与 与 |
| C、二甲苯与乙苯 |
| D、2,2-二甲基丙烷与新戊烷 |






