题目内容
8.废旧印刷电路板的回收利用可实现资源再生,并减少污染.废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末.(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是BD(填字母).
A.热裂解形成燃油
B.露天焚烧
C.作为有机复合建筑材料的原料
D.直接填埋
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g)△H=64.39KJ•mol-1
2H2O2(l)=2H2O(l)+O2(g)△H=-196.46KJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.84KJ•mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为Cu(s)+H2O2 (l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1.
(3)在298K下,C、Al的单质各1mol完全燃烧,分别放出热量aKJ和bKJ.又知一定条件下,Al能将C从CO2置换出来,写出此置换反应的热化学方程式4Al(s)+3CO2(g)=3C(s)+2Al2O3(s)△H=(3a-4b)kJ/mol.
分析 (1)处理印刷电路板非金属粉末时不会产生污染环境的物质,则符合环境保护理念;
(2)根据已知的热化学反应方程式和盖斯定律来分析Cu与H2O2反应生成Cu2+和H2O的热化学方程式;
(3)依据在298K下,C、Al的单质各1mol完全燃烧,分别放出热量aKJ和bKJ和盖斯定律计算得到所需热化学方程式:4Al(s)+3CO2(g)=3C(s)+2Al2O3(s)的反应热.
解答 解:(1)因热裂解形成燃油及作为有机复合建筑材料的原料都可实现资源的再利用,露天焚烧能生成有害气体则污染空气,直接填埋则废旧印刷电路板中的重金属离子会污染土壤,所以不符合环境保护理念的是BD;
故答案为:BD;
(2)由①Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)H1=64.39KJ•mol-1;
②2H2O2(l)═2H2O(l)+O2(g)H2=-196.46KJ•mol-1;
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)H3=-285.84KJ•mol-1;
则反应Cu(s)+H2O2 (l)+2H+(aq)=Cu2+(aq)+2H2O(l)可由反应①+②×$\frac{1}{2}$+③得到,
由盖斯定律可知该反应的反应热△H=H1+H2×$\frac{1}{2}$+H3=64.39KJ•mol-1+(-196.46KJ•mol-1)×$\frac{1}{2}$+(-285.84KJ•mol-1)=-319.68KJ.mol-1,
故答案为:Cu(s)+H2O2 (l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1;
(3)由题意可写出热化学方程式:
①C(s)+O2(g)═CO2(g)△H=-a kJ•mol-1,
②4Al(s)+3O2(g)═2Al2O3(s)△H=-4b kJ•mol-1.
高温下铝置换碳的反应为:4Al+3CO2$\frac{\underline{\;高温\;}}{\;}$2Al2O3+3C,
根据盖斯定律:②-①×3可得,4Al(s)+3CO2(g)=3C(s)+2Al2O3(s),△H=(3a-4b)kJ/mol.
故答案为:4Al(s)+3CO2(g)=3C(s)+2Al2O3(s),△H=(3a-4b)kJ/mol.
点评 本题以废旧印刷电路板的回收利用为载体,考查了热化学方程式、环境保护等知识,熟悉热化学方程式书写注意问题,明确盖斯定律计算反应热的方法是解题关键,题目难度不大.

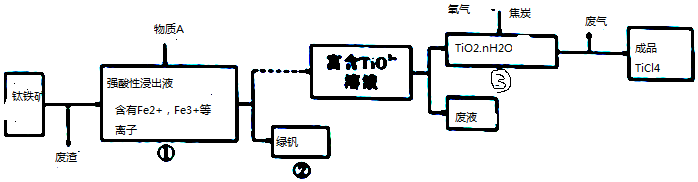
(1)FeTiO3中,Ti元素的化合价为+4.
(2)往①中加入的物质A是Fe.
(3)②中的绿矾带有棕黄色,原因可能是含有Fe3+;设计实验证明Fe3+杂质离子的存在取样,溶于水,向溶液中加入KSCN溶液,如果溶液变为血红色,证明含有Fe3+;
(4)写出③中TiO2和过量焦炭、氯气在高温下反应的化学方程式:TiO2+2C+Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO.
(5)用金属Mg还原成品TiO4得到Mg、MgCl2和Ti的混合物,再真空蒸馏制备Ti. 依据下表,蒸馏温度略高于1412℃即可.
| Mg | MgCl2 | Ti | |
| 熔点/℃ | 648.0 | 714 | 1667 |
| 沸点/℃ | 1090 | 1412 | 3287 |
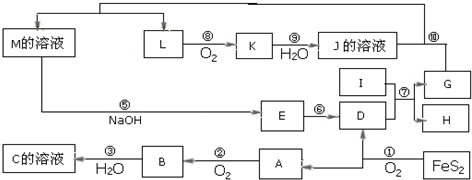
(7)向含有Fe2+、Fe3+溶液加入适量KOH和油脂,在高速撞拌下得到磁流体材料KxFeO2.
①若x=l.请写出在酸性条件下KxFeO2溶液与足量KI溶液反应的离子方程式:8H++2FeO2-+2I-=2Fe2++I2+4H2O.
②磁流体材料KxFeO2在组成上可理解为aK2O•bFeO•cFe2O3,若x=1.3,则b:c=6:7.
| A. | 任何化学反应都伴随着能量的变化 | |
| B. | H2O(g)→H2O(l)该过程放出大量的热,所以该过程是化学变化 | |
| C. | 化学反应中能量的变化一定都表现为热量的变化 | |
| D. | 氢氧化钡晶体和氯化铵晶体的反应属于放热反应 |
| A. | 有毒的 | B. | 单质 | C. | 氧化物 | D. | 金属或合金 |
| A. | 汽车尾气的大量排放--光化学污染 | |
| B. | 含磷洗衣粉的大量使用--水体富营养化 | |
| C. | 生活污水任意排放--CO2浓度增大 | |
| D. | 氟氯烃的大量使用--臭氧空洞 |
| A. | 分子式C7H16的烃,分子中有4个甲基的同分异构体有4种(不考虑立体异构) | |
| B. | 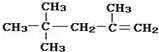 的名称为:2,2,4-三甲基-4-戊烯 的名称为:2,2,4-三甲基-4-戊烯 | |
| C. | 化合物 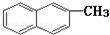 是苯的同系物 是苯的同系物 | |
| D. | 植物油的主要成分是不饱和高级脂肪酸 |