题目内容
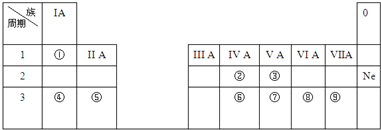
3.下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素.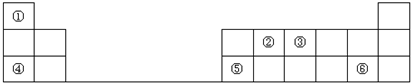
请按要求回答下列问题:
(1)写出②的元素名称碳;④的单质与水反应的化学方程式2Na+2H2O=2NaOH+H2↑
(2)将④、⑤和⑥三种元素相比较,金属性最强的是Na(填元素符号);
(3)元素③的最高价氧化物对应的水化物的化学式为HNO3;
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式NH3+HCl=NH4Cl.
(5)④与⑥两元素组成的化合物的电子式:
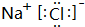
(6)⑤的氧化物的水化物与④的氧化物的水化物能反应 (填“能”或“不能”)
分析 由元素在周期表中的位置可知,①为H、②为C、③为N、④为Na、⑤为Al、⑥为Cl.
(1)钠与水反应生成氢氧化钠与氢气;
(2)同周期自左而右金属性减弱;
(3)元素③的最高价氧化物对应的水化物为硝酸;
(4)氨气与氯化氢生成NH4Cl固体;
(5)④与⑥两元素组成的化合物为NaCl,由钠离子与氯离子构成;
(6)④、⑤的氧化物的水化物分别为氢氧化钠、氢氧化铝,二者反应生成偏铝酸钠与水.
解答 解:由元素在周期表中的位置可知,①为H、②为C、③为N、④为Na、⑤为Al、⑥为Cl.
(1)②的元素名称为碳,钠与水反应生成氢氧化钠与氢气,反应方程式为2Na+2H2O=2NaOH+H2↑,故答案为:碳;2Na+2H2O=2NaOH+H2↑;
(2)同周期自左而右金属性减弱,故金属性最强为Na,故答案为:Na;
(3)元素③的最高价氧化物对应的水化物为硝酸,化学式为HNO3,故答案为:HNO3;
(4)氨气与氯化氢生成NH4Cl固体,反应方程式为:NH3+HCl=NH4Cl,故答案为:NH3+HCl=NH4Cl;
(5)④与⑥两元素组成的化合物为NaCl,由钠离子与氯离子构成,电子式为: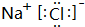 ,故答案为:
,故答案为: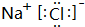 ;
;
(6)④、⑤的氧化物的水化物分别为氢氧化钠、氢氧化铝,二者反应生成偏铝酸钠与水,故答案为:能.
点评 本题考查元素周期表与元素周期律综合运用,题目基础性、贴近教材,熟练掌握元素周期律表的结构.

练习册系列答案
相关题目
14.下列物质能与金属钠、碳酸氢钠溶液、碳酸钠溶液都能反应的是( )
| A. | 苯酚 | B. | 苯甲酸 | C. | 苯甲醛 | D. | 乙二醇 |
18.下列说法不正确的是( )
| A. | 食品保存在冰箱中不易坏,说明温度对反应速率有影响 | |
| B. | 在金属与非金属的分界线附近寻找半导体材料 | |
| C. | 在周期表中,第IA族全部为金属元素 | |
| D. | 金刚石与石墨互为同素异形体 |
12.下列物质中,含有非极性共价键的是( )
| A. | CaCl2 | B. | CO2 | C. | Na2O2 | D. | CH4 |
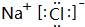 ;
;
 H2O
H2O C2H4
C2H4 .
.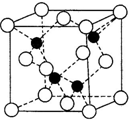 已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增.B原子的P轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3P轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体.根据以上信息,回答下列问题:
已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增.B原子的P轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3P轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体.根据以上信息,回答下列问题: