题目内容
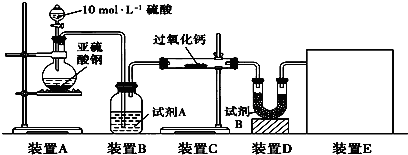
过氧化钙(CaO2)难溶于水,常温下稳定,在潮湿空气及水中缓慢放出氧气,广泛应用于渔业等领域.下图是以大理石(主要杂质Fe2O3)等为原料制取CaO2的流程:

(1)操作①中应包括
A溶解 B.过滤 C.蒸馏 D.分液 E.蒸发结晶
请写CaCO3 和稀盐酸反应的离子方程式:
(2)用氨水调节pH至8-9的目的:
(3)从滤液C中可回收得到的工业产品的化学式为
(4)操作②的化学反应方程式:

(1)操作①中应包括
A、B、E
A、B、E
(填序号).A溶解 B.过滤 C.蒸馏 D.分液 E.蒸发结晶
请写CaCO3 和稀盐酸反应的离子方程式:
CaCO3+2H+=Ca2++CO2↑+H2O
CaCO3+2H+=Ca2++CO2↑+H2O
.(2)用氨水调节pH至8-9的目的:
除去Fe3+ (或使Fe3+转化为Fe(OH)3沉淀被除去)
除去Fe3+ (或使Fe3+转化为Fe(OH)3沉淀被除去)
.(3)从滤液C中可回收得到的工业产品的化学式为
NH4NO3
NH4NO3
.(4)操作②的化学反应方程式:
CaCl2+H2O2=CaO2↓+2HCl
CaCl2+H2O2=CaO2↓+2HCl
.分析:(1)实现固体和液体的分离采用过滤的方法,从氯化钙的溶液中获得氯化钙的结晶水合物要采用蒸发结晶的方法,碳酸钙能和强酸反应;
(2)pH至8-9范围段内时,三价铁可易形成沉淀;
(3)硝酸钙和碳酸铵之间可以发生复分解反应生成碳酸钙和硝酸铵;
(4)双氧水可以和氯化钙反应生成过氧化钙和盐酸.
(2)pH至8-9范围段内时,三价铁可易形成沉淀;
(3)硝酸钙和碳酸铵之间可以发生复分解反应生成碳酸钙和硝酸铵;
(4)双氧水可以和氯化钙反应生成过氧化钙和盐酸.
解答:解:根据图示信息,可得出:滤液A的成分有硝酸钙和硝酸铁以及剩余的硝酸,当pH至8-9范围段内时,三价铁可易形成沉淀,所以滤渣B是氢氧化铁,滤液B是硝酸钙,和碳酸铵之间可以发生复分解反应生成碳酸钙和硝酸铵,过滤,沉淀碳酸钙用盐酸溶解然后蒸发结晶可以得到氯化钙晶体,再失水成为无水氯化钙,双氧水可以和氯化钙反应生成过氧化钙和盐酸.
(1)碳酸钙和硝酸铵的混合物过滤后,所得沉淀碳酸钙用盐酸溶解然后蒸发结晶可以得到氯化钙晶体,CaCO3 和稀盐酸反应的实质是:CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:A、B、E,CaCO3+2H+=Ca2++CO2↑+H2O;
(2)用氨水调节pH至8-9,三价铁可易形成沉淀,从而分离出硝酸钙溶液,故答案为:除去Fe3+ (或使Fe3+转化为Fe(OH)3沉淀被除去);
(3)硝酸钙和碳酸铵之间可以发生复分解反应生成碳酸钙和硝酸铵,过滤所得滤液主要成分是硝酸铵,故答案为:NH4NO3;
(4)双氧水可以和氯化钙反应生成过氧化钙和盐酸,即CaCl2+H2O2=CaO2↓+2HCl,故答案为:CaCl2+H2O2=CaO2↓+2HCl.
(1)碳酸钙和硝酸铵的混合物过滤后,所得沉淀碳酸钙用盐酸溶解然后蒸发结晶可以得到氯化钙晶体,CaCO3 和稀盐酸反应的实质是:CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:A、B、E,CaCO3+2H+=Ca2++CO2↑+H2O;
(2)用氨水调节pH至8-9,三价铁可易形成沉淀,从而分离出硝酸钙溶液,故答案为:除去Fe3+ (或使Fe3+转化为Fe(OH)3沉淀被除去);
(3)硝酸钙和碳酸铵之间可以发生复分解反应生成碳酸钙和硝酸铵,过滤所得滤液主要成分是硝酸铵,故答案为:NH4NO3;
(4)双氧水可以和氯化钙反应生成过氧化钙和盐酸,即CaCl2+H2O2=CaO2↓+2HCl,故答案为:CaCl2+H2O2=CaO2↓+2HCl.
点评:本题是一道框图推断题,考查知识面较广,要求学生具有分析和解决问题的能力,难度较大.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
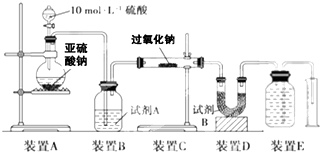



 CaO2+2HCl
CaO2+2HCl