题目内容
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是

①C;②H2O2;③Na;④Fe;⑤HNO3
A.仅①③④????? ?? B.仅①②⑤
C.仅①②③⑤?? ?? D.①②③④⑤
【答案】
D
【解析】
试题分析:运用代入法进行判断①若甲是C,与O2反应可能生成CO或CO2,则乙、丙分别为CO、CO2,CO与O2反应可生成CO2,CO2与C反应可生成CO,正确;②若甲是H2O2,H2O2分解可得H2O和O2,则乙、丙分别为H2O、O2,H2O电解可得O2,O2与H2反应可得H2O,正确;③若甲是Na,钠与Cl2反应可生成NaCl,Na与H2O反应可生成NaOH,则乙、丙可能是NaCl、NaOH,NaOH与HCl反应可生成NaCl,用惰性电极电解NaCl溶液可生成NaOH,正确;④若甲是Fe,Fe在Cl2中燃烧生成FeCl3,Fe与HCl反应可生成FeCl2,则乙、丙可能是FeCl2、FeCl3,FeCl2与Cl2反应生成FeCl3,FeCl3与Fe反应可生成FeCl2,正确;⑤若甲为HNO3,HNO3与Cu反应可生成NO或NO2,则乙、丙可能是NO、NO2,NO与O2反应生成NO2,NO2与H2O反应生成NO,正确,故D项正确。
考点:本题考查物质的化学性质及相互转化。

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
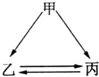 如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )①C ②H2O2 ③Na ④Fe ⑤HNO3.
| A、仅①③④ | B、仅①②⑤ | C、仅①②③⑤ | D、①②③④⑤ |
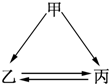 如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是①Fe;②HNO3;③Na;④C( )
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是①Fe;②HNO3;③Na;④C( )| A、①②③ | B、②③④ | C、①②④ | D、①②③④ |
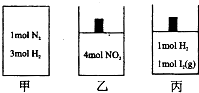 如图所示的甲、乙、丙三个绝热容器中分别发生的反应为:
如图所示的甲、乙、丙三个绝热容器中分别发生的反应为:甲:N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol
乙:2NO2(g)?N2O4
丙:H2(g)+I2(g)?2HI(g)
则下列有关说法不正确的是( )
| A、若甲的体积为2L,经过10秒后反应达到平衡状态,放出热量为55.44U,则H2的反应速率是0.09mol/(L?s) | B、若甲、乙中反应达到平衡时的体积相同,则两容器中所含物质的量可能相同 | C、若乙、丙中反应达到平衡时的体积、压强均相同,则乙中NO2的转化率为50% | D、若甲、乙、丙中反应均达到平衡状态时,则甲中物质的平均相对分子质量不变,乙中物质的颜色不变,丙中的温度不变 |
