题目内容
在标准状况下,将SO2,HCl,H2组成的混和气体4.48L通过足量的NaOH溶液,溶液的质量增加6.85g,从溶液中逸出的气体经干燥后体积为1.12L,则原混和气体中 SO2的体积为( )
| A、0.224 L | B、1.12 L | C、3、36L. | D、4L |
分析:在标准状况下,将SO2,HCl,H2组成的混和气体通过足量的NaOH溶液,SO2,HCl被吸收,氢气逸出,故氢气的体积为1.12L,溶液增重为6.85g为SO2、HCl的总质量,根据混合气体总体积,可知SO2、HCl的体积之和=4.48L-1.12L=3.36L,再列方程计算.
解答:解:在标准状况下,将SO2,HCl,H2组成的混和气体通过足量的NaOH溶液,SO2,HCl被吸收,氢气逸出,故氢气的体积为1.12L,溶液增重为6.85g为SO2、HCl的总质量,根据混合气体总体积,可知SO2、HCl的体积之和=4.48L-1.12L=3.36L,
令SO2的物质的量为xmol、HCl的物质的量为ymol,由题意得:
解得:x=0.05、y=0.1,
故标况下,混合气体中SO2的体积=0.05mol×22.4L/mol=1.12L,
故选B.
令SO2的物质的量为xmol、HCl的物质的量为ymol,由题意得:
|
解得:x=0.05、y=0.1,
故标况下,混合气体中SO2的体积=0.05mol×22.4L/mol=1.12L,
故选B.
点评:本题考查混合物计算,难度不大,理解发生的反应是解题关键,侧重对基础知识的巩固.

练习册系列答案
相关题目
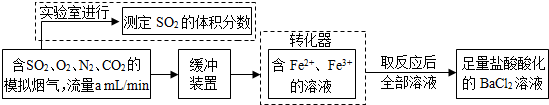

 的浓度为
的浓度为
 =BaSO4↓+2H2O
=BaSO4↓+2H2O