题目内容
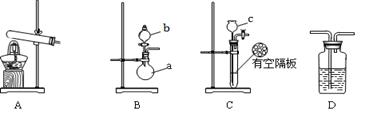
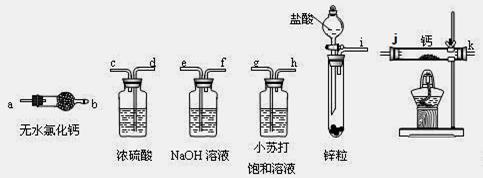
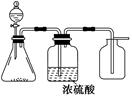
下列装置所示的实验中,能达到实验目的的是
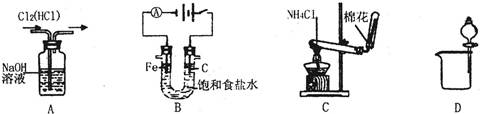

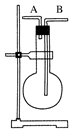
| A.除去Cl2中的HCl | B.电解制氯气和氢气 |
| C.实验室制氨气 | D.分离碘酒中的碘和酒精 |
B
试题分析:NaOH易与HCl反应中和反应,也易与Cl2发生氧化还原反应,既除去杂质,又除去被提纯的氯气,说明选择的除杂试剂不合理,HCl易溶于饱和食盐水,Cl2难溶于饱和食盐水,应选择饱和食盐水洗气除去杂质,故A错误;读图可知,C作阳极,Fe作阴极,Clˉ、OHˉ移向阳极,还原性较强的Clˉ优先失去电子,发生氧化反应,放出氯气,而H+、Na+移向阴极,氧化性较强的H+得到电子,发生还原反应,放出氢气,故B正确;NH4Cl固体受热易分解为氨气和氯化氢气体,而NH3与HCl遇冷易化合为氯化铵固体,因为缺少与HCl中和的强碱固体,不能用加热氯化铵固体的方法制取氨气,故C错误;I2易溶于酒精,不能分层,不能用萃取、分液的方法分离碘酒,应根据二者的沸点不同,用蒸馏法进行分离,故D错误。

练习册系列答案
相关题目