题目内容
已知A为常见的金属单质,根据下图所示的关系回答下列问题:
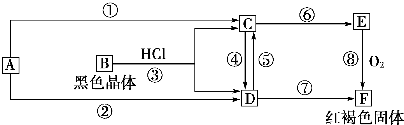
(1)确定B、D、E的化学式,B为
(2)写出⑧的化学方程式及④、⑤的离子方程式:

(1)确定B、D、E的化学式,B为
Fe3O4
Fe3O4
,D为FeCl3
FeCl3
,E为Fe(OH)2
Fe(OH)2
.(2)写出⑧的化学方程式及④、⑤的离子方程式:
4Fe(OH)2+O2+2H2O═4Fe(OH)3
4Fe(OH)2+O2+2H2O═4Fe(OH)3
,2Fe2++Cl2═2Fe3++2Cl-
2Fe2++Cl2═2Fe3++2Cl-
,Fe+2Fe3+═3Fe2+
Fe+2Fe3+═3Fe2+
.分析:E被氧气氧化生成红褐色固体F,则F是Fe(OH)3,E是Fe(OH)2,根据元素守恒知,A单质是Fe,黑色晶体B和盐酸反应生成C和D,A能发生反应生成C和D,B是黑色晶体且含有铁元素,能和盐酸反应生成两种不同的盐,则B是Fe3O4,C是FeCl2,D为FeCl3,结合物质的性质分析解答.
解答:解:E被氧气氧化生成红褐色固体F,则F是Fe(OH)3,E是Fe(OH)2,根据元素守恒知,A单质是Fe,黑色晶体B和盐酸反应生成C和D,A能发生反应生成C和D,B是黑色晶体且含有铁元素,能和盐酸反应生成两种不同的盐,则B是Fe3O4,C是FeCl2,D为FeCl3,
(1)通过以上分析知,B、D、E分别是Fe3O4、FeCl3、Fe(OH)2,
故答案为:Fe3O4;FeCl3;Fe(OH)2;
(2)F是Fe(OH)3,E是Fe(OH)2,氢氧化亚铁不稳定易被氧气氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,C是氯化亚铁,D是氯化铁,氯化亚铁和氯气反应生成氯化铁,离子反应方程式为:2Fe2++Cl2═2Fe3++2Cl-,氯化铁和铁反应生成氯化亚铁,离子反应方程式为:Fe+2Fe3+═3Fe2+,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;2Fe2++Cl2═2Fe3++2Cl-;Fe+2Fe3+═3Fe2+.
(1)通过以上分析知,B、D、E分别是Fe3O4、FeCl3、Fe(OH)2,
故答案为:Fe3O4;FeCl3;Fe(OH)2;
(2)F是Fe(OH)3,E是Fe(OH)2,氢氧化亚铁不稳定易被氧气氧化生成氢氧化铁,反应方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,C是氯化亚铁,D是氯化铁,氯化亚铁和氯气反应生成氯化铁,离子反应方程式为:2Fe2++Cl2═2Fe3++2Cl-,氯化铁和铁反应生成氯化亚铁,离子反应方程式为:Fe+2Fe3+═3Fe2+,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;2Fe2++Cl2═2Fe3++2Cl-;Fe+2Fe3+═3Fe2+.
点评:本题以铁及其化合物为载体考查了无机物的推断,以“红褐色固体”为突破口采用正逆结合的方法进行推断,“铁三角”是常考查点,亚铁离子、铁离子的检验也是常考查点,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 ”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“ ”表示氢原子,小黑点“
”表示氢原子,小黑点“

