题目内容
(1)已知16克A和20克B恰好完全反应生成0.05mol C和30克D,则C的摩尔质量为_________(2)0.3mol氨气和0.4mol二氧化碳的质量___________(填“相等”或“不相等”,下 同),
同),
所含原子数____________。
(3)4 g H2与22.4 L(标准状况)CO2相比,所含分子数目较多的是____________。
(4)3.01×1023个CO2分子中含 mol氧原子,在标准状况下其体积为 L,它与 g H2O含有相同的氧原子数。
(5)写出下列物质的电离方程式:硫酸铵__________ ____;氢氧化钡_______ ___。
练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
14.X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如图所示:
请回答下列问题:
(1)W元素在周期表中的位置第三周期第VIIA族.
(2)X、Y、Z、W分别形成的简单离子的半径由小到大的顺序为O2-<N3-<Cl-<S2-(用化学式填写,下同);Y、Z对应的气态氢化物的稳定性H2O>H2S.
(3)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡时有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式为2SO2(g)+O2(g)?2SO3(g)△H=-190.0kJ•mol-1.
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式2S2Cl2+2H2O=SO2+3S+4HCl.
| X | Y | |
| Z | W |
(1)W元素在周期表中的位置第三周期第VIIA族.
(2)X、Y、Z、W分别形成的简单离子的半径由小到大的顺序为O2-<N3-<Cl-<S2-(用化学式填写,下同);Y、Z对应的气态氢化物的稳定性H2O>H2S.
(3)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡时有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式为2SO2(g)+O2(g)?2SO3(g)△H=-190.0kJ•mol-1.
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式2S2Cl2+2H2O=SO2+3S+4HCl.
15.在容积一定的密闭容器中,可逆反应A(g)+B(g)?xC(g),有如图所示的关系曲线,根据下图下列判断正确的是( )
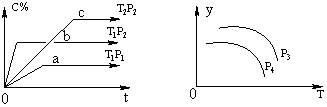

| A. | p3>p4,y轴表示A的物质的量分数 | |
| B. | 若增大A的浓度,平衡体系颜色加深,C一定是有颜色的气体 | |
| C. | p3<p4,y轴表示平衡常数K | |
| D. | p3>p4,y轴表示混合气体的平均摩尔质量 |
某探究性学习小组拟通过锌与盐酸的反应研究影响反应速率的因素.
该探究性学习小组用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如表所示:
实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
Ⅰ | 薄片 | 15 | 200 |
Ⅱ | 薄片 | 25 | 90 |
Ⅲ | 粉末 | 25 | 10 |
(1)该实验的目的是探究 、 对锌和稀盐酸反应速率的影响;
(2)实验Ⅰ和Ⅱ表明 ,化学反应速率越大;
(3)能表明固体的表面积对反应速率有影响的实验编号是 和 ,实验结论是 ;
(4)请设计一个实验方案证明盐酸的浓度对该反应的速率的影响: .
18.常温下,下列各组离子在有一定关限定条件下的溶液中一定能大量共存的是( )
| A. | 由水电离产生的c(H+)=10-12 mol•L一1的溶液中:K+、Na+、Fe2+、NO3- | |
| B. | 常温下,pH=7的溶液中:Al3+、Cl-、HCO3-、SO42- | |
| C. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、Cu2+、S2-、Cl- | |
| D. | pH=1的溶液中:Fe3+、NO3-、SO42-、Na+ |

