题目内容
实验室制Cl2的反应为4HCl(浓)+MnO2 = MnCl2+C12↑+2H2O,下列说法错误的是
A.还原剂是HCl,氧化剂是MnO2
B.每生成1 molCl2,转移电子的物质的量为2 mol
C.每消耗1 molMnO2,起还原剂作用的HCl消耗4mol
D.生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质
C
【解析】
试题分析:A.在实验室制Cl2的反应为4HCl(浓)+MnO2 = MnCl2+C12↑+2H2O中,HCl中的Cl元素的化合价升高,失去电子,所以HCl是还原剂,而MnO2中的Mn元素的化合价降低,得到电子,所以MnO2是氧化剂,故选项A正确;B.根据电子转移数目相等可知:每生成1 molCl2,转移电子的物质的量为2 mol,选项B正确;有方程式可知:每消耗1 molMnO2,反应消耗HCl是4mol,其中起还原剂作用的HCl消耗2mol,错误;D.由于反应是在溶液中进行的,盐酸有挥发性,所以在生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质,正确。
考点:考查实验室制Cl2的反应原理及反应产物的成分的确定的知识。

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
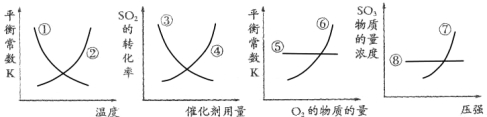
 2SO3(g) △H<0,反应达到平衡后,改变某一个条件,下列示意图曲线①~⑧中正确的是
2SO3(g) △H<0,反应达到平衡后,改变某一个条件,下列示意图曲线①~⑧中正确的是