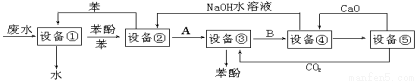
��Ŀ����
��16�֣�
��1��С���������о��¶ȶԷ�Ӧ���ʵ�Ӱ�족ʵ��ʱ��������֧�Թܾ�����4mL 0.01mol/L��KMnO4������Һ��2mL 0.1mol/L H2C2O4���Ҷ��ᣩ��Һ����A�Թ�������ˮ�У� B�Թ�������ˮ�У���¼��Һ��ɫ�����ʱ�䡣
����Ҫ�� ���ữKMnO4��Һ����ɫ����ʱ��tA tB���>������=����<������
��д���÷�Ӧ�����ӷ���ʽ ��
��2��ʵ������ƿ������ɳ���Ҷ�����Ʒ��С�����������Ӧ��ԭ�����ⶨ�京�����������Ϊ��
������250 mL��Һ��ȷ����5.000g�Ҷ�����Ʒ�����250mL��Һ��
�ڵζ���ȷ��ȡ25.00 mL������Һ����ƿ�У����������ữ����0.1000 mol��L-1 KMnO4��Һװ�� �����ʽ����ʽ�����ζ��ܣ����еζ�������
��ʵ���з��֣��յ�������KMnO4��Һʱ����ҺѸ�ٱ���Ϻ�ɫ������ƿҡ��һ��ʱ����Ϻ�ɫ������ʧ���ټ����μ�ʱ���Ϻ�ɫ�ͺܿ���ɫ�ˡ������ԭ�� ���� ��֤���ﵽ�ζ��յ㡣
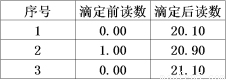
�ۼ��㣺 �ظ���������2�Σ���¼ʵ���������±���������KMnO4��Һ��ƽ�����Ϊ mL������Ʒ�Ĵ���Ϊ ������֪H2C2O4����Է�������Ϊ90��
�������������в����ᵼ�²ⶨ���ƫ�ߵ��� ��
A��δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ��� B���ζ�ǰ��ƿ������ˮ
C���ζ�ǰ�ζ��ܼ��첿�������ݣ��ζ���������ʧ D����С�Ľ���������KMnO4��Һ������ƿ��
E���۲����ʱ���ζ�ǰ���ӣ��ζ�����
��1�������ᣬ<����5H2C2O4+2MnO4-+6H+=10CO2+2Mn2++8H2O����2������ʽ����Ӧ�����ɵ�Mn2+���д����ã����������ɫ��ӿ죻�������һ������KMnO4��Һ����ƿ����Һ����ɫ��Ϊdz�Ϻ�ɫ���Ұ�����ڲ���ɫ����20.00mL��90.00%����A��C��D��
��������
�����������1��������������ǿ�������ԣ������ữKMnO4��Һ�������л�ԭ�ԣ��ᱻKMnO4��Һ�����������Ҫ�������ữKMnO4��Һ�������¶����ߣ���ѧ��Ӧ���ʼӿ죬���Է�Ӧʱ���Խ�̣������ɫ����ʱ��tA<tB; �ڸ��ݵ����غ㡢����غ㼰ԭ���غ�ɵø÷�Ӧ�����ӷ���ʽ��5H2C2O4+2MnO4-+ 6H+=10CO2+2Mn2++8H2O����2����KMnO4��Һ��ǿ�����ԣ��ḯʴ������KMnO4��ҺӦ��װ����ʽ�ζ����У���ʵ���з��֣��յ�������KMnO4��Һʱ����ҺѸ�ٱ���Ϻ�ɫ������ƿҡ��һ��ʱ����Ϻ�ɫ������ʧ���ټ����μ�ʱ���Ϻ�ɫ�ͺܿ���ɫ�˿��ܵ�ԭ���Ƿ�Ӧ�����ɵ�Mn2+���д����ã����������ɫ��ӿ죻���������һ������KMnO4��Һ����ƿ����Һ����ɫ��Ϊdz�Ϻ�ɫ���Ұ�����ڲ���ɫ���۷���3��ʵ���������ݣ���֪�����������̫��Ҫ��ȥ�����ĵ�KMnO4��Һ�������V(KMnO4)=(20.10+19.90)ml��2=20.00ml��n(KMnO4)= 0.1000 mol/L �� 0.020 L=2��10-3mol;���ݷ���ʽ��֪n(H2C2O4)= 5/2 n(KMnO4)= 5/2��2��10-3mol=5��10-3mol������H2C2O4��������m=5��10-3mol ��90g/mol=0.45g,���Բ���Ĵ�����0.45g��(5.000g��10) �� 100%=90.00%����A��δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ��ܣ������Һ��Ũ��ƫС�������ĵ����ƫ�������IJ�������ʵ���ƫ����ȷ��B���ζ�ǰ��ƿ������ˮ����������κ�Ӱ�죬����C���ζ�ǰ�ζ��ܼ��첿�������ݣ��ζ���������ʧ�������ĵı���Һ���ƫ�����Լ���IJ����Ũ�Ⱦ�ƫ�ߣ���ȷ��D����С�Ľ���������KMnO4��Һ������ƿ�⣬�����ĵı���Һ���ƫ�࣬ʹ�����Ũ��ƫ�ߣ���ȷ��E���۲����ʱ���ζ�ǰ���ӣ��ζ����ӣ������ĵı���Һ���ƫС�������Dz�����Һ��Ũ��ƫС������
���㣺����ζ����������ʵ���Ũ�ȵļ����е�Ӧ�á������������ӷ���ʽ����д��֪ʶ��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����˵����ȷ���� 
A��ij��Ӧ�ķ�Ӧ�����������仯����ͼ��ʾ��������ͼ������֪�������ı䷴Ӧ���ʱ�
B��������Na������O2��Ӧ����Na2O�����¶���������Na2O�������ӿ�
C����֪��
���ۼ� | C��C | C=C | C��H | H��H |
����/ kJ��mol-1 | 348 | 610 | 413 | 436 |
����Լ������Ӧ  �Ħ�HΪ��384 kJ��mol-1
�Ħ�HΪ��384 kJ��mol-1
D. ��������0.10 mol��L-1�İ�ˮ�м�������NH4Cl���壬NH3��H2O�ĵ���̶Ⱥ���Һ��pH����С