题目内容
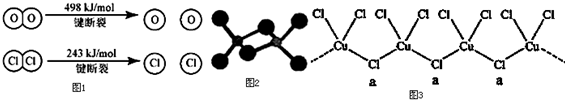
(1)已知在一定条件下的反应4HCl+O2=2Cl2+2H2O中,有4mol HCl被氧化时,放出120kJ的热量,且
则断开1mol H-O 键与断开 1mol H-Cl 键所需能量相差为 KJ.
(2)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是 .
(3)已知AlCl3熔点190℃,沸点183℃,结构如图2所示:AlCl3晶体内含有的作用力有 (填序号).
A.离子键 B.共价键 C.金属键D.配位键 E.范德华力 F.氢键
(4)氯和钾与不同价态的铜可生成两种化合物,这两种化合物中的阴离子均为无限长链结构(如图3),a位置上Cl原子的杂化轨道类型为 ,已知其中一种化合物的化学式为KCuCl3,另一种的化学式为 .
则断开1mol H-O 键与断开 1mol H-Cl 键所需能量相差为
(2)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ?mol-1) | 786 | 715 | 3401 |
(3)已知AlCl3熔点190℃,沸点183℃,结构如图2所示:AlCl3晶体内含有的作用力有
A.离子键 B.共价键 C.金属键D.配位键 E.范德华力 F.氢键
(4)氯和钾与不同价态的铜可生成两种化合物,这两种化合物中的阴离子均为无限长链结构(如图3),a位置上Cl原子的杂化轨道类型为

考点:晶体的类型与物质熔点、硬度、导电性等的关系,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)据△H=反应物键能和-生成物键能和,据此计算H-O键与H-Cl键的键能差,进而计算断开1mol H-O键与断开1mol H-Cl键所需能量差;
(2)晶格能越大物质的熔点越高,通过比较NaCl和KCl的晶格能可见,结构相似时,影响晶体晶格能大小的因素有离子半径以及离子所带电荷的多少;
(3)根据离子晶体和分子晶体的熔点关系分析,Al最外层3个电子,可知成键个数,据此分析;
(4)a位置上Cl原子成2个单键,含有2对孤对电子,杂化轨道数为4,据此判断;一种化合物的化学式为KCuCl3,其中铜元素为+2价,故另一种化合物中铜为+1价,阴离子构成与CuCl3一样,但CuCl3原子团的化合价为-2,据此书写.
(2)晶格能越大物质的熔点越高,通过比较NaCl和KCl的晶格能可见,结构相似时,影响晶体晶格能大小的因素有离子半径以及离子所带电荷的多少;
(3)根据离子晶体和分子晶体的熔点关系分析,Al最外层3个电子,可知成键个数,据此分析;
(4)a位置上Cl原子成2个单键,含有2对孤对电子,杂化轨道数为4,据此判断;一种化合物的化学式为KCuCl3,其中铜元素为+2价,故另一种化合物中铜为+1价,阴离子构成与CuCl3一样,但CuCl3原子团的化合价为-2,据此书写.
解答:
解:(1)E(H-O)、E(HCl)分别表示H-O键能、H-Cl键能,
反应A中,4mol HCl被氧化,放出115.6kJ的热量,反应热△H=反应物总键能-生成物的总键能,故:
4×E(H-Cl)+498kJ/mol-[2×243kJ/mol+4×E(H-O)]=-120KJ/mol,
故断开1mol H-O键与断开1mol H-Cl键所需能量相差约为33kJ/mol×1mol=33kJ,
故答案为:33;
(2)离子半径Mg2+<Na+<O2-<Ca2+<Cl-;离子电荷数Na+=Cl-<O2-=Mg2+=Ca2+,离子晶体的离子半径越小,带电荷数越多,晶格能越大,则晶体的熔沸点越高,则有NaCl、KCl、MgO、CaO熔点由高到低的顺序是MgO>CaO>NaCl>KCl,故答案为:MgO>CaO>NaCl>KCl;
(3)分子晶体熔点一般较低,所以AlCl3为分子晶体,应有极性共价键,又Al最外层只有3个电子,Al成四键结构,应有一个配位键,分子晶体内有分子间作用力,也就是范德华力,故选:BDE;
(4)a位置上Cl原子成2个单键,含有2对孤对电子,杂化轨道数为4,杂化轨道类型为sp3,一种化合物的化学式为KCuCl3,其中铜元素为+2价,故另一种化合物中铜为+1价,阴离子构成与CuCl3一样,但CuCl3原子团的化合价为-2,其化学式为:K2CuCl3;
故答案为:sp3;K2CuCl3.
反应A中,4mol HCl被氧化,放出115.6kJ的热量,反应热△H=反应物总键能-生成物的总键能,故:
4×E(H-Cl)+498kJ/mol-[2×243kJ/mol+4×E(H-O)]=-120KJ/mol,
故断开1mol H-O键与断开1mol H-Cl键所需能量相差约为33kJ/mol×1mol=33kJ,
故答案为:33;
(2)离子半径Mg2+<Na+<O2-<Ca2+<Cl-;离子电荷数Na+=Cl-<O2-=Mg2+=Ca2+,离子晶体的离子半径越小,带电荷数越多,晶格能越大,则晶体的熔沸点越高,则有NaCl、KCl、MgO、CaO熔点由高到低的顺序是MgO>CaO>NaCl>KCl,故答案为:MgO>CaO>NaCl>KCl;
(3)分子晶体熔点一般较低,所以AlCl3为分子晶体,应有极性共价键,又Al最外层只有3个电子,Al成四键结构,应有一个配位键,分子晶体内有分子间作用力,也就是范德华力,故选:BDE;
(4)a位置上Cl原子成2个单键,含有2对孤对电子,杂化轨道数为4,杂化轨道类型为sp3,一种化合物的化学式为KCuCl3,其中铜元素为+2价,故另一种化合物中铜为+1价,阴离子构成与CuCl3一样,但CuCl3原子团的化合价为-2,其化学式为:K2CuCl3;
故答案为:sp3;K2CuCl3.
点评:本题考查了利用键能计算焓变的方法、影响晶格能大小的因素及晶格能对熔点的影响和分子晶体的相关知识,题目难度不大,注意知识的积累.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
工业上获得大量的乙烯、丙烯、1,3-丁二烯采用的方法是( )
| A、煤高温干馏 | B、石油减压分馏 |
| C、石油裂化 | D、石油裂解 |
下列物质中,不可用来漂白、杀菌消毒的是( )
| A、次氯酸钠 | B、过氧化钠 |
| C、氯水 | D、含碘食盐 |
下列说法不正确的是( )
| A、Ksp只与难溶电解质的性质和温度有关 |
| B、由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C、任意两种难溶电解质作比较时,Ksp小的,溶解度一定小 |
| D、t℃时,Ksp(CaCO3)=4×10-16,则CaCO3饱和溶液中c(Ca2+)=2×10-8 mol/L |
设在密闭容器中进行下列反应C(固)+CO2(气)?2CO(气)反应速率为 v1;CO(气)+NO2(气)?CO2(气)+NO(气)反应速率为 v2对于上述反应,恒温时增大压强,v1和v2的变化情况为( )
| A、v1、v2都增大 |
| B、v1增大,v2不变 |
| C、v1增大,v2减小 |
| D、无法确定 |
下列各式属于正确的水解反应的离子方程式的是( )
| A、HCO3-+H2O?CO32-+H3O+ |
| B、S2-+H2O?H2S+2OH- |
| C、Fe3++3H2O?Fe(OH)3+3H+ |
| D、CH3COOH+OH-?CH3COO-+H2O |
加水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
A、
| ||
B、
| ||
| C、c(H+)?c(OH-) | ||
| D、n(OH-) |
下列说法不正确的是( )
| A、浓硫酸能与铜反应释放出氢气 |
| B、浓硫酸能与灼热的木炭反应,生成二氧化碳和二氧化硫 |
| C、浓硫酸具有吸水性,在实验中常用作干燥剂 |
| D、冷的浓硫酸可以用铁质或铝质容器储存 |
改变下列某一条件:①浓度 ②压强 ③温度 ④催化剂,其中一定能使化学平衡发生移动的是( )
| A、①④ | B、②③ | C、①③ | D、②④ |