题目内容
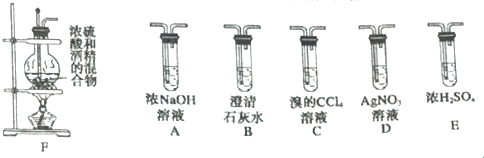
12.检验淀粉、蛋白质、葡萄糖溶液,依次可分别使用的试剂和对应的现象正确的是( )| A. | 碘水,变蓝色;浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀 | |
| B. | 浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀;碘水,变蓝色 | |
| C. | 新制Cu(OH)2,砖红色沉淀;碘水,变蓝色;浓硝酸,变黄色 | |
| D. | 碘水,变蓝色;新制Cu(OH)2,砖红色沉淀;浓硝酸,变黄色 |
分析 淀粉遇碘单质变蓝,可利用碘水来鉴别淀粉,蛋白质遇浓硝酸变黄,葡萄糖溶液在碱性条件下与新制Cu(OH)2悬浊液共热生成砖红色沉淀,以此解答该题.
解答 解:①因淀粉遇碘单质变蓝,可利用碘水来鉴别;
②蛋白质遇浓硝酸变黄,可用浓硝酸鉴别;
③葡萄糖溶液在碱性条件下与新制Cu(OH)2悬浊液共热生成砖红色沉淀.
故选A.
点评 本题考查有机物的检验和鉴别,为高频考点,侧重于学生的分析、实验和评价能力的考查,注意把握物质的性质的异同以及特征反应现象,难度不大.

练习册系列答案
相关题目
2.据报道,有一种叫Thibacillus Ferroxidans的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐.发生的反应为:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中Fe的化合价为+2,上述反应中被氧化的元素是Fe和CuFeS2中的S.
(2)工业生产中利用上述反应后的溶液,按如图甲流程可制备胆矾(CuSO4•5H2O):
①分析表格(其中KSP是相应金属氢氧化物的沉淀溶解平衡常数):
步骤一应调节溶液的pH范围是3.2≤pH<4.7.请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因加入CuO与H+反应使c(H+)减小,c(OH-)增大,使溶液中c(Fe3+)•c3(OH-)>Ksp[Fe(OH)3],导致Fe3+生成沉淀而除去.
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶.
(3)有人提出可以利用图乙的装置从溶液B中提炼金属铜.该过程中图乙电极的反应式是4OH--4e-=O2↑+2H2O,总反应的方程式是2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+2H2SO4+O2↑.
(1)CuFeS2中Fe的化合价为+2,上述反应中被氧化的元素是Fe和CuFeS2中的S.
(2)工业生产中利用上述反应后的溶液,按如图甲流程可制备胆矾(CuSO4•5H2O):

①分析表格(其中KSP是相应金属氢氧化物的沉淀溶解平衡常数):
| Ksp | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.6×10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶.
(3)有人提出可以利用图乙的装置从溶液B中提炼金属铜.该过程中图乙电极的反应式是4OH--4e-=O2↑+2H2O,总反应的方程式是2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+2H2SO4+O2↑.
7.五种短周期元素X、Y、Z、W、M,X的质子总数与电子层数相同,Y、Z、W、M在周期表中的位置如图所示,其中W的单质是一种重要的半导体材料.下列说法不正确的是( )
| Y | Z | M |
| W |
| A. | 原子半径大小关系为:W>Y>Z>M>X | |
| B. | 最高价氧化物对应的水化物酸性:W<Y<Z | |
| C. | 分子式为X5YZM2的化合物中含有离子键和共价键 | |
| D. | 元素Y、W的单质一定属于同种类型的晶体 |
17.下列说法不正确的是( )
| A. | 水晶有固定的熔点,而普通玻璃则没有 | |
| B. | 水泥、玻璃、陶瓷属于传统的无机非金属材料 | |
| C. | 不锈钢和普通钢的组成元素完全相同,但耐腐蚀性能不同 | |
| D. | 氯化铵和单质碘在加热时有类似现象,但本质不同 |
4.过氧化氢(O为-1价)在二氧化锰催化作用下分解放出氧气的反应机理如下:
①MnO2+H2O2+2H+=Mn2++O2↑+2H2O
②Mn2++H2O2=MnO2+2H+
下列说法正确的是( )
①MnO2+H2O2+2H+=Mn2++O2↑+2H2O
②Mn2++H2O2=MnO2+2H+
下列说法正确的是( )
| A. | H2O2在①中是氧化剂,在②中是还原剂 | |
| B. | 在①中每生成1 mol O2,转移的电子数为1.204×1024 | |
| C. | Mn2+在①中是还原产物,在②中是氧化产物 | |
| D. | 在二氧化锰催化作用下,1 mol H2O2分解生成22.4 L O2 |
1.下列关于有机化合物的说法正确的是( )
| A. | 甲烷和乙烯都可以与氯气反应 | |
| B. | 酸性高锰酸钾可以氧化苯和甲苯 | |
| C. | 乙烯可以与氢气发生加成反应,苯不能与氢气加成 | |
| D. | 溴乙烷在NaOH的醇溶液中充分反应可得到乙醇 |
2.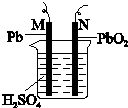 已知铅蓄电池的反应原理是:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(l)△H<0图为铅蓄电池的示意图.下列说法正确的是( )
已知铅蓄电池的反应原理是:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(l)△H<0图为铅蓄电池的示意图.下列说法正确的是( )
 已知铅蓄电池的反应原理是:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(l)△H<0图为铅蓄电池的示意图.下列说法正确的是( )
已知铅蓄电池的反应原理是:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(l)△H<0图为铅蓄电池的示意图.下列说法正确的是( )| A. | 充电时,阳极的电极反应式为:PbSO4+2e-═Pb+SO42- | |
| B. | 充电时,若N连接电源正极,则该极生成PbO2 | |
| C. | 放电时,c(H2SO4)不变,两极的质量增加 | |
| D. | 放电时,N为负极,其电极反应式为:PbO2+SO42-+4H++2e-═PbSO4+2H2O |