题目内容
下列离子方程式的书写中,正确的是( )
| A、铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-═NH3↑+H2O |
| C、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| D、碳酸氢钠溶液中滴入稀盐酸:HCO3-+H+═CO2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.不符合反应的客观事实,铁与盐酸反应生成二价铁离子;
B.漏掉碳酸氢根离子与氢氧根离子的反应;
C.一水合氨是弱电解质,保留化学式;
D.碳酸氢钠溶液中滴入稀盐酸生成二氧化碳、氯化钠和水.
B.漏掉碳酸氢根离子与氢氧根离子的反应;
C.一水合氨是弱电解质,保留化学式;
D.碳酸氢钠溶液中滴入稀盐酸生成二氧化碳、氯化钠和水.
解答:
解:A.铁与盐酸反应的离子方程式:Fe+2H+═Fe2++H2↑,故A错误;
B.NH4HCO3溶液与过量NaOH溶液反应的离子方程式为:NH4++HCO3-+2OH-=NH3?H2O+H2O+CO32-,故B错误;
C.AlCl3溶液中加入足量的氨水离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故C错误;
D.碳酸氢钠溶液中滴入稀盐酸反应的离子方程式为:HCO3-+H+═CO2↑+H2O,故D正确;
故选:D.
B.NH4HCO3溶液与过量NaOH溶液反应的离子方程式为:NH4++HCO3-+2OH-=NH3?H2O+H2O+CO32-,故B错误;
C.AlCl3溶液中加入足量的氨水离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故C错误;
D.碳酸氢钠溶液中滴入稀盐酸反应的离子方程式为:HCO3-+H+═CO2↑+H2O,故D正确;
故选:D.
点评:本题考查了离子方程式的书写及书写正误的判断,题目难度不大,注意化学式拆分的原则,易错选项为B,书写离子方程式时,注意不能漏掉反应的离子.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列说法错误的是( )
A、按照系统命名法, 的名称为3,3,4-三甲基己烷 的名称为3,3,4-三甲基己烷 |
| B、乙醇、乙酸和乙酸乙酯可以用饱和Na2CO3溶液鉴别 |
| C、苯乙烯中所有原子可能共平面 |
D、1.0mol的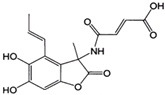 与NaOH溶液和Br2反应时,分别需要消耗NaOH 5.0mol和Br2 3.0mol 与NaOH溶液和Br2反应时,分别需要消耗NaOH 5.0mol和Br2 3.0mol |
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流.电池总反应为:4Al+3O2+6H2O═4Al(OH)3,下列说法不正确的是( )
| A、正极反应式为:O2+2H2O+4e-═40H - |
| B、电池工作时,电流由铝电极沿导线流向铂电极 |
| C、以网状的铂为正极,可增大与氧气的接触面积 |
| D、该电池通常只需更换铝板就可继续使用 |
下列说法正确的是( )
| A、吸热反应一定要加热才能发生 |
| B、在5mL 0.1mol?L-1的KI溶液中加入5滴0.1mol?L-1 FeCl3溶液,充分震荡后,取少量混合液液加入几滴KSCN溶液,溶液显红色 |
| C、一定温度下,在某容器中进行可逆反应:C(s)+H2O(g)?CO(g)+H2(g),只要增大压强,反应速率一定加快 |
| D、电解氯化钠溶液可制得金属钠 |
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:

有关上述反应物和产物的叙述正确的是( )

有关上述反应物和产物的叙述正确的是( )
| A、按碳的骨架分类,上述三种有机物均属于芳香烃 |
| B、乙酰水杨酸分子中不存在手性碳原子 |
| C、在核磁共振氢谱中,对乙酰氨基酚分子有4个峰 |
| D、贝诺酯分子中有3种不同类型的含氧官能团 |
化学已渗透到人类生活的各个方面.下列说法不正确的是( )
| A、凡含有食品添加剂的食物对人体健康均有害,不可食用 |
| B、地沟油的主要成分是高级脂肪酸甘油酯,处理后可用于制肥皂 |
| C、钻石、水晶、刚玉都是人们熟知的宝石,但其化学成分不同 |
| D、低盐低脂饮食是目前大力提倡的健康饮食方法,可有效预防高血压等疾病 |
下列离子在指定条件下一定能大量共存的是( )
| A、滴入酚酞溶液显红色的溶液中:K+、Na+、Cu2+、SO42- |
| B、与铝反应产生氢气的溶液中:Na+、AlO2-、NO3-、HCO3- |
| C、水电离产生的c(H+)=10-13 mol?L-1的溶液中:Na+、Cl-、NO3-、SO42- |
| D、0.1mol?L-1 HNO3溶液中:Mg2+、NH4+、Fe2+、Cl- |
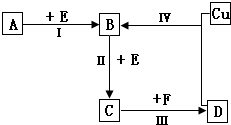 有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题: