题目内容
13.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )| A. | SO2和SiO2 | B. | CO2和H2 | C. | NaCl和HCl | D. | CCl4和KCl |
分析 根据晶体的类型和所含化学键的类型分析,离子化合物含有离子键,可能含有共价键,共价化合物只含共价键,双原子分子或多原子分子含有共价键,由此分析解答.
解答 解:A、SO2和SiO2分别是由共价键形成的分子和原子晶体,所以化学键类型相同,而晶体类型不同,故A不符;
B、CO2和H2都是由共价键形成的分子晶体,所以化学键类型、晶体类型都相同,故B符和;
C、NaCl和HCl分别是由离子键、共价键形成的离子晶体和分子晶体,所以化学键类型、晶体类型都不相同,故C不符;
D、CCl4和KCl分别是由共价键、离子键形成的分子晶体和离子晶体,所以化学键类型、晶体类型都不相同,故D不符;
故选:B.
点评 本题考察了化学键类型和晶体类型的关系,判断依据为:离子晶体中阴阳离子以离子键结合,原子晶体中原子以共价键结合,分子晶体中分子之间以范德华力结合,分子内部存在化学键.

练习册系列答案
相关题目
4.醇在浓硫酸作用且加热条件下,醇分子间发生脱水生成醚.CH3CH2-O-CH2CH3).用浓硫酸与分子式分别为C2H6O和C3H8O的醇的混合液反应,可以得到醚的种类有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
1.只用一种试剂鉴别甲酸、乙醇、乙酸、葡萄糖四种溶液,可选用( )
| A. | 钠 | B. | 酸性高锰酸钾 | C. | 溴水 | D. | 新制氢氧化铜 |
8.下列说法正确的是( )
| A. | 物质发生化学反应都伴随着能量变化,但不一定会引起状态的变化 | |
| B. | 伴随着能量变化的物质变化都是化学变化 | |
| C. | 反应物的总能量低于反应产物的总能量,此反应需加热才进行 | |
| D. | 反应物的总能量高于反应产物的总能量,此反应在任何条件下都可进行 |
18. 如图所示是Zn和Cu形成的原电池,下列描述合理的是( )
如图所示是Zn和Cu形成的原电池,下列描述合理的是( )
①Zn为负极,Cu为正极
②Cu极上有气泡产生
③阳离子移向Zn极
④电子从Zn极流出沿导线流向Cu极
⑤该装置能将电能转化为化学能
⑥若有0.5mol电子流经导线,则负极质量减轻16g.
 如图所示是Zn和Cu形成的原电池,下列描述合理的是( )
如图所示是Zn和Cu形成的原电池,下列描述合理的是( )①Zn为负极,Cu为正极
②Cu极上有气泡产生
③阳离子移向Zn极
④电子从Zn极流出沿导线流向Cu极
⑤该装置能将电能转化为化学能
⑥若有0.5mol电子流经导线,则负极质量减轻16g.
| A. | ①②④ | B. | ②③ | C. | ④⑤⑥ | D. | ③④⑤ |
2.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 46gNO2和N2O4的混气体中,含氮原子数目是NA | |
| B. | 1.0L 0.1mol/L的NaF溶液中,含F-离子数目是0.1NA | |
| C. | 11.2L的H2中,含有的电子数目是NA | |
| D. | 1molFeCl3跟沸水完全反应转化为氢氧化铁胶体,其中胶体粒子的数目是NA |
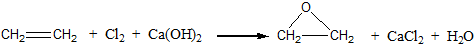
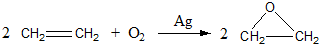
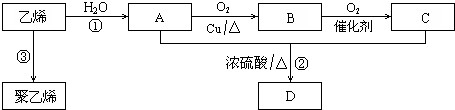
 ;反应类型:加聚反应.
;反应类型:加聚反应.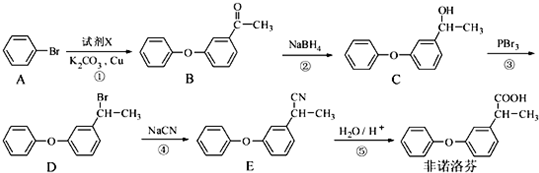
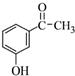 .
.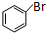 +2NaOH$\stackrel{一定条件}{→}$
+2NaOH$\stackrel{一定条件}{→}$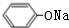 +NaBr+H2O.
+NaBr+H2O.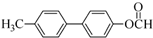 .
.