题目内容
1.CH4与O2的质量比为1:4时极易爆炸,此时.CH4与O2的物质的量比为( )| A. | 1:1 | B. | 1:4 | C. | 1:2 | D. | 2:1 |
分析 令甲烷与氧气的质量分别为1g、4g,根据n=$\frac{m}{M}$计算甲烷、氧气的物质的量,据此计算判断.
解答 解:甲烷与氧气的质量比为1:4,令甲烷与氧气的质量分别为1g、4g,则:
lg甲烷的物质的量为$\frac{1g}{16g/mol}$=$\frac{1}{16}$mol,
4g氧气的物质的量为$\frac{4g}{32g/mol}$=$\frac{1}{8}$mol.
同温同压下,甲烷与氧气的物质的量之比为$\frac{1}{16}$mol:$\frac{1}{8}$mol=1:2.
故选:C.
点评 本题考查了有关物质的量计算,熟悉以物质的量为核心的计算公式是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.金属单质与足量Cl2反应后,生成物的化学式中,不正确的是( )
| A. | FeCl2 | B. | NaCl | C. | FeCl3 | D. | CuCl2 |
12.化学与生活、生产、环境等社会实际密切相关.下列叙述正确的是( )
| A. | 酒精浓度越高消毒效果愈好 | |
| B. | 涤纶、塑料、光导纤维都是有机高分子材料 | |
| C. | 用电镀厂的废水直接灌溉农田,可提高水的利用率 | |
| D. | 外形似海绵、密度小、有磁性的碳与石墨互为同素异形体 |
16.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 在同温同压时,相同体积的任何气体单质所含的分子数目相同 | |
| B. | 2g氢气所含原子数目为NA | |
| C. | 在常温常压下,11.2L氮气所含的原子数目为NA | |
| D. | 17g氨气所含氢原子数目为NA |
6.将KNO3、NaCl和沙子的混合物分开,必要的操作步骤是( )
| A. | 过滤、蒸馏、萃取 | B. | 溶解、过滤、结晶 | C. | 分液、溶液、萃取 | D. | 过滤、结晶、升华 |
13.现有下列4组物质:
A. CaO、MgO、CO2、CuO
B.H2、Cl2、N2、Cu
C.O2、Fe、Cu、Zn
D.HCl、H2O、H2SO4、HNO3
(1)填写下表空白
(2)若(1)表中的4种物质相互作用可生成一种新物质--碱式碳酸铜[化学式为Cu2(OH)2CO3],请写出该反应的化学方程式:2Cu+O2+CO2+H2O═Cu2(OH)2CO3.
A. CaO、MgO、CO2、CuO
B.H2、Cl2、N2、Cu
C.O2、Fe、Cu、Zn
D.HCl、H2O、H2SO4、HNO3
(1)填写下表空白
| A组 | B组 | C组 | D组 | |
| 分类标准 | 金属氧化物 | 金属单质 | ||
| 不属于该类别的物质 | Cu | H2O |
15.下列实验不能做为判断依据的是( )
| A. | 根据钠和镁分别与冷水的反应情况,判断钠和镁金属性的强弱 | |
| B. | 根据氯水与溴化钠溶液的反应情况,判断氯和溴非金属性的强弱 | |
| C. | 根据HF和HCl的水溶液的酸性强弱,判断氟与氯非金属的强弱 | |
| D. | 根据Na+和K+的氧化性的强弱,判断钠和钾的金属性的强弱 |
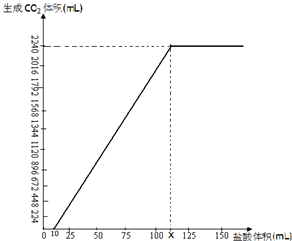 NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:Na2CO3+nH2O→Na2CO3•nH2O(n为平均值,n≤10).取没有妥善保管的NaHCO3样品A9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如右图.(已知盐酸滴加至10mL时,开始产生气体,加至15mL时生成CO2112mL,溶解的CO2忽然不计)
NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:Na2CO3+nH2O→Na2CO3•nH2O(n为平均值,n≤10).取没有妥善保管的NaHCO3样品A9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如右图.(已知盐酸滴加至10mL时,开始产生气体,加至15mL时生成CO2112mL,溶解的CO2忽然不计) 有5瓶白色固体试剂,分别是BaCl2、NaOH、Mg(OH)2、Na2CO3、BaCO3.现分别取少量试剂进行下列实验.请回答下列问题:
有5瓶白色固体试剂,分别是BaCl2、NaOH、Mg(OH)2、Na2CO3、BaCO3.现分别取少量试剂进行下列实验.请回答下列问题: