题目内容
9.填写下列空白:(1)写出表示含有8个质子、8个中子的原子的化学符号:816O.其在周期表中的位置为第二周期VIA族.
(2)元素周期表中最活泼的非金属元素位于第17纵行.
(3)在NaCl、NaOH、N2、H2S中,只含有极性键的是H2S,只含有离子键的是NaCl,既含有极性键又含有离子键的是NaOH.
分析 (1)含有8个质子、8个中子的原子为C,其质量数为13;根据电子排布判断在周期表中的位置;
(2)周期表中最活泼非金属元素为F;
(3)一般不同非金属元素之间形成极性键,同种非金属元素之间形成非极性键,活泼金属元素与活泼非金属元素之间形成离子键,据此分析.
解答 解:(1)含有8个质子、8个中子的原子为O,其质量数为16,原子的化学符号为816O,O原子核外有8个电子分两层排布,最外层有6个电子,所以在周期表中位于第二周期第VIA族;
故答案为:816O;二;VIA;
(2)周期表中最活泼非金属元素为F,周期表共18个纵行,则最活泼非金属元素位于第17纵行,
故答案为:17;
(3)NaCl中只含有离子键;
NaOH中含有离子键和极性共价键;
N2中只含有非极性键;
H2S中只含有极性键;
所以只含有极性键的是H2S;只含有离子键的是NaCl;既含有极性键又含有离子键的是NaOH,
故答案为:H2S;NaCl;NaOH.
点评 本题考查元素周期表的结构及应用、化学键,把握周期表结构及元素的位置、元素的种类为解答的关键,侧重基础知识的考查,(5)为解答的易错点,题目难度不大.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
19.化学与生产、生活密切相关.下列说法或做法正确的是( )
| A. | 将废弃的塑料袋回收进行露天焚烧,以解决“白色污染”问题 | |
| B. | 煤的干馏和石油的分馏均属于化学变化 | |
| C. | 用浸泡过的高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的 | |
| D. | 福尔马林用于保存海鲜产品 |
4.对一些具有危险的化学物质,若要在其包装上贴危险化学品标记,下列标签贴错的是( )
| A. |  浓硫酸 | B. |  汽油 | C. |  KNO3 | D. |  乙醇 |
18.下列说法正确的是( )
| A. | P2O5可用于干燥Cl2和NH3 | |
| B. | 用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2 | |
| C. | 通过浓硫酸除去HCl中的H2O | |
| D. | 通过灼热的CuO除去H2中的CO |
19.下列叙述正确的是( )
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| B. | 溶于水后能电离出氢离子的化合物一定是酸 | |
| C. | 硫酸钡难溶于水,但硫酸钡属于电解质 | |
| D. | 氯气溶于水后的溶液能导电,故氯气属于电解质 |
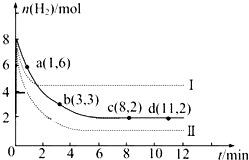 工业上“固定”和利用CO2能有效地减轻“温室”效应,可用CO2生产燃料甲醇:
工业上“固定”和利用CO2能有效地减轻“温室”效应,可用CO2生产燃料甲醇: A、B、C、D均为含苯环的有机物,且式量B>A>C.
A、B、C、D均为含苯环的有机物,且式量B>A>C. .
. .
. 、
、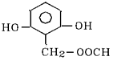 、
、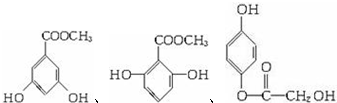 (其中的任意2种).
(其中的任意2种).