题目内容
某化合物A的化学式为C5H11Cl,分析数据表明,分子中有2个“—CH2—”、2个“—CH3”、1个“
解析:
| 解析:本题有2种解法。构造法和条件变换法。
方法1(构造法):先构造出有机物结构式中间部分,即先用2个二价甲基“—CH2—”和1个三价甲基“ 然后,再往(Ⅰ)式和(Ⅱ)式上安排结构中数目较少的取代基,即—Cl(氯原子),得到以下4种结构: 最后,分别在①~④的结构中安排2个—CH3,可得答案。 方法2(条件变换法):C5H11Cl是C5H12被1个Cl原子取代的产物,求C5H11Cl的同分异构体,就是求C5H12一氯代物的同分异构体——戊基种数。本题解法如下。 先写出C5H12的同分异构体: 然后观察(Ⅰ)、(Ⅱ)、(Ⅲ)中H的不同位置(①~⑧),并在其不同位置上安排“—Cl”,保留符合题意(2个“—CH2—”,2个“—CH3”、1个“
|

 开心快乐假期作业暑假作业西安出版社系列答案
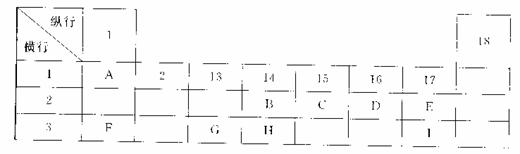
开心快乐假期作业暑假作业西安出版社系列答案下列为元素周期表的一部分,表中阿拉伯数字(1、2……)是原周期表中行或列的序号。请参照元素A~I在表中的位置,回答下列问题。
|
(1)B、C两元素中非金属性较强的是 (写出元素名称),请设计一个简单的实验证明这一结论 。
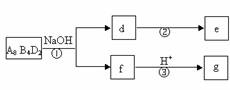
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子反应方程式
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成离子个数比为1:1和1:2的两种离子化合物Z和M。写出Z与Y反应的化学方程式: 。
(4)I元素在周期表里的位置在第 周期、第 族。
实验室中采用右图所示装置模拟工业上同时制取元素A和I
的单质过程: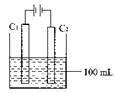
①写出电极C1上发生反应的电极反应式 。
②当电极上产生112mL(标准状况)元素I单质气体时(假设气体完全逸出,溶液体积不变),烧杯中溶液的pH= 。(![]() )
)