题目内容
13.亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组欲通过下面的实验装置制备NaNO2并进行相关的检验.
查阅资料得知:
①2NO+Na2O2=2NaNO2
②2NO2+Na2O2=2NaNO3
(1)写出装置A烧瓶中发生反应的化学方程式并标出电子转移的方向和数目
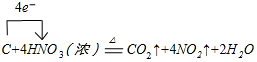 .
.(2)B装置的作用是将NO2转化为NO,同时铜与稀硝酸反应生成NO.
(3)写出D中处理尾气的离子反应方程式5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O.
(4)有同学认为装置C中产物不仅有亚硝酸钠,还有其它的固体产物,为制备纯净的NaNO2应在B、C装置间增加一个装置,写出装置及盛放试剂的名称盛放碱石灰的干燥管(或U形管).
(5)NaNO2又称“工业盐”,其外观与NaCl相似,有咸味,毒性较强,了解两种物质的鉴别方法尤为重要.将上述实验得到的产品配成溶液完成下列实验,写出所加试剂及观察到的现象. 可供选择的试剂有:稀H2SO4,酸性KMnO4溶液,FeCl2溶液,KSCN溶液,淀粉KI溶液.
①利用HNO2的不稳定性.已知:2HNO2=NO2↑+NO↑+H2O 向取样溶液中加入稀H2SO4,产生红棕色气体.
②利用NO2-的还原性:向取样溶液中加入酸性KMnO4溶液,紫色褪去.
③利用NO2-的氧化性:向取样溶液中加入FeCl2溶液和KSCN溶液,溶液变红(或淀粉KI溶液,溶液变蓝).
分析 制备NaNO2并对其性质作探究,由实验装置可知,A中发生C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,B中B装置中NO2与水反应生成NO,同时铜与稀硝酸反应也生成NO,C中发生2NO+Na2O2═2NaNO2,D中高锰酸钾吸收尾气NO,
(1)装置A烧瓶中,碳和浓硝酸反应生成二氧化碳、二氧化氮和水,方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
(2)B装置中,NO2与水反应生成NO,同时铜与稀硝酸反应也生成NO;
(3)D中高锰酸钾氧化NO生成 硝酸根离子,高锰酸根离子被还原成锰离子;
(4)有同学认为装置c中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,那么NO中混有CO2、NO2,可以在B、C之间增加装有碱石灰或生石灰的装置E,以吸收杂质CO2、NO2;
(5)NaNO2在酸性条件下不稳定,生成红棕色的二氧化氮,NaNO2具有还原性,能使高锰酸钾溶液褪色,NaNO2具有氧化性,能将亚铁离子氧化成铁离子,或者将碘离子氧化成碘单质,据此答题.
解答 解:(1)装置A烧瓶中,碳和浓硝酸反应生成二氧化碳、二氧化氮和水,反应的化学方程式并标出电子转移的方向和数目为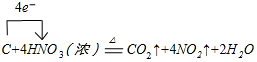 ,
,
故答案为: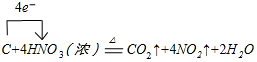 ;
;
(2)B装置中,NO2与水反应生成NO,同时铜与稀硝酸反应也生成NO,故答案为:将NO2转化为NO,同时铜与稀硝酸反应生成NO;
(3)D中高锰酸钾氧化NO生成 硝酸根离子,高锰酸根离子被还原成锰离子,反应的离子方程式为5NO+3MnO4-+4H+=5 NO3-+3Mn2++2H2O,
故答案为:5NO+3MnO4-+4H+=5 NO3-+3Mn2++2H2O;
(4)有同学认为装置c中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,那么NO中混有CO2、NO2,可以在B、C之间增加装有盛放碱石灰的干燥管(或U形管),以吸收杂质CO2、NO2,
故答案为:盛放碱石灰的干燥管(或U形管);
(5)NaNO2在酸性条件下不稳定,生成红棕色的二氧化氮,NaNO2具有还原性,能使高锰酸钾溶液褪色,NaNO2具有氧化性,能将亚铁离子氧化成铁离子,或者将碘离子氧化成碘单质,
①利用HNO2的不稳定性,向取样溶液中加入稀H2SO4,观察到的现象是产生红棕色气体;
②利用NO2-的还原性,向取样溶液中加入酸性KMnO4溶液,观察到的现象是酸性KMnO4溶液;
③利用NO2-的氧化性,向取样溶液中加入FeCl2溶液和KSCN溶液,观察到的现象是溶液变红,或者向取样溶液中加入淀粉KI溶液,观察到的现象是溶液变蓝,
故答案为:①稀H2SO4,产生红棕色气体; ②酸性KMnO4溶液,紫色褪去;③FeCl2溶液和KSCN溶液,溶液变红(或淀粉KI溶液,溶液变蓝).
点评 本题是一道实验方案的设计和探究题,考查学生分析和解决问题的能力,综合性强,难度大.

| A. | Cu2+ Fe2+ NO3- Cl- | B. | K+ Mg2+HCO3-SO42- | ||
| C. | S2- Na+ K+、Cl- | D. | Ba2+Na+ I- NO3- |
| A. | 98gH2SO4 | B. | 56gFe | C. | 44.8LHCI | D. | 6gH2 |
 氮的化合物在生产生活中广泛存在.
氮的化合物在生产生活中广泛存在.(1)①氯胺(NH2Cl)的电子式为
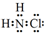 .可通过反应NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g)制备氯胺,已知部分化学键的键能如表所示(假定不同物质中同种化学键的键能一样),则上述反应的△H=+11.3kJ•mol-1.
.可通过反应NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g)制备氯胺,已知部分化学键的键能如表所示(假定不同物质中同种化学键的键能一样),则上述反应的△H=+11.3kJ•mol-1.| 化学键 | 键能/(kJ•mol-1) |
| N-H | 391.3 |
| Cl-Cl | 243.0 |
| N-Cl | 191.2 |
| H-Cl | 431.8 |
(2)用焦炭还原NO的反应为:2NO(g)+C(s)?N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=0.003mol•L-1•min-1.
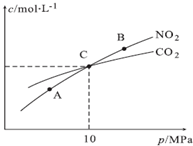
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s)?N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
①A、B两点的浓度平衡常数关系:Kc(A)=Kc(B)(填“<”或“>”或“=”).
②A、B、C三点中NO2的转化率最高的是A(填“A”或“B”或“C”)点.
| 化合物 | 密度(g•cm-3) | 水溶性 | 沸点(℃) |
| 冰乙酸 | 1.05 | 易溶 | 118.1 |
| 正丁醇 | 0.80 | 微溶 | 117.2 |
| 正丁醚 | 0.77 | 不溶 | 142.0 |
| 乙酸正丁酯 | 0.90 | 微溶 | 126.5 |
(一)合成:
方案甲:采用装置甲,在烧瓶中加入11.5mL正丁醇、7.2mL冰醋酸、3~4滴浓硫酸和沸石,摇匀.安装好带分水器的回流反应装置,通冷却水,加热.在反应过程中通过分水器下部的旋塞分出生成的水.反应基本完成后,停止加热.
方案乙:采用装置乙,加料方式与方案甲相同.加热回流,反应60min后停止加热.

(二)提纯:甲乙两方案提纯方法均如下:

回答下列问题:
(1)a处水流方向是进水(填“进水”或“出水”),仪器b的名称(直形)冷凝管.
(2)合成步骤中,判断方案甲酯化反应已基本完成的标志是分水器中水不再生成或分水器中的水层不再增加时.
(3)提纯过程中,步骤②是为了除去有机层中残留的酸,检验有机层已呈中性的操作是用玻璃棒蘸取有机层,点在pH试纸上,与标准比色卡对照,读取pH值判断;步骤③的目的是除去溶于酯中的少量无机盐.
(4)下列有关洗涤过程中分液漏斗的使用正确的是BC(选填序号).
a.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
b.洗涤时振摇放气操作应如图戊所示
c.放出下层液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
d.洗涤完成后,先放出下层液体,然后继续从下口放出有机层置于干燥的锥形瓶中
(5)按装置丙蒸馏,最后圆底烧瓶中残留的液体主要是正丁醚;若按图丁放置温度计,则收集到的产品馏分中还含有正丁醇.
(6)实验中乙酸丁酯产率较高的方案是方案甲,理由是通过分水器及时分离出产物水,有利于酯化反应的进行,提高酯的产率.
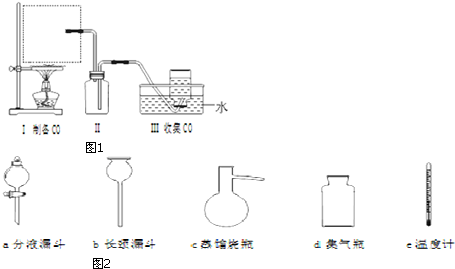
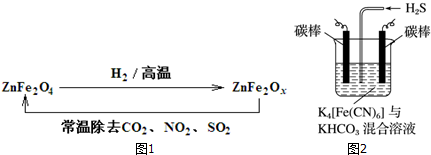
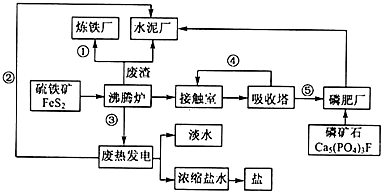 生态工业园区的建设,不仅仅是体现环保理念,重要依据循环经济理论和充分考虑经济的可持续发展,如图是某企业设计的硫酸-磷铵-水泥联产,海水-淡水多用,盐-热-电联产生三大生态产业链流程图.
生态工业园区的建设,不仅仅是体现环保理念,重要依据循环经济理论和充分考虑经济的可持续发展,如图是某企业设计的硫酸-磷铵-水泥联产,海水-淡水多用,盐-热-电联产生三大生态产业链流程图. 云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.请回答下列问题:
云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.请回答下列问题: