题目内容
10.7g氯化铵与足量氢氧化钙混合共热,问最多可以制得标准状况下的氨气多少升? .
考点:化学方程式的有关计算
专题:计算题
分析:氯化铵固体和熟石灰混合加热生成氨气、水和氯化钙;根据方程式中定量关系计算生成氨气的体积.
解答:
解:10.7g氯化铵的物质的量为
=0.2mol,则:
2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O
2mol 44.8L
0.2mol V
所以V=
=4.48L,
故答案为:4.48L.
| 10.7g |
| 53.5g/mol |
2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O
2mol 44.8L
0.2mol V
所以V=
| 0.2mol×44.8L |
| 2mol |
故答案为:4.48L.
点评:本题考查根据方程式的计算,比较基础,侧重学生对基础知识的巩固.要注意计算格式,方程式中各量应符合上下一致,左右对应即可,即g、mol、L单位对应.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
NH3与HCl相遇,可观察到的现象是( )
| A、产生白雾 |
| B、产生白烟 |
| C、产生棕黄色的烟 |
| D、无明显现象 |
下列有机物命名正确的是( )
A、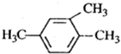 1,3,4-三甲苯 |
B、 2-氯丙烷 |
C、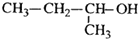 1-甲基-1-丙醇 |
D、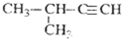 2-甲基-3-丁炔 |
 的分子式是
的分子式是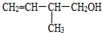 .该有机物中所含官能团的名称是
.该有机物中所含官能团的名称是