题目内容
根据碘与氢气反应的热化学方程式(碘为气态或固态),下列判断正确的是
(ⅰ)I2(?)+H2(g)  2HI(g)+9.48 kJ (ⅱ)I2(?)+H2(g)
2HI(g)+9.48 kJ (ⅱ)I2(?)+H2(g)  2HI(g)-26.48 kJ
2HI(g)-26.48 kJ
A.ⅰ中碘为气态,ⅱ中碘为固态
B.反应(ⅰ)的产物比反应(ⅱ)的产物稳定
C.1 mol I2(g)中通入1 mol H2(g),反应放热9.48 kJ
D.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
A
【解析】
试题分析:A由于产物的能量相同,是放热反应,ⅱ是吸热反应,说明反应物含有的ⅰ中的高。因此ⅰ中碘为气态,ⅱ中碘为固态,正确;B.物质含有的能量越低,物质的稳定性就越强。由于反应(ⅰ)的产物与反应(ⅱ)的产物状态相同,因此稳定性相同,错误;C.1 mol I2(g)中通入1 mol H2(g),发生反应,由于该反应是可逆反应,物质不能完全转化,所以放热小于9.48 kJ ,错误;D.1 mol固态碘与1 mol气态碘所含的能量相差26.48 kJ +9.48 kJ =35.96 kJ,错误。
考点:考查物质状态的确定、物质含有的能量与反应热、物质的稳定性的关系的知识。

练习册系列答案
相关题目
中学实验室为完成下列实验通常选择的装置正确的是
A | B | C | D | |
实验 | 用CCl4萃取 溴水中的溴 | 从NaCl与I2的混合物中回收I2 | 制备与收集二氧化硫 | 制备乙酸丁酯 |
装置 |
|
|
|
|
 )是最简单的芳香胺,暴露于空气中变为棕色,该变化最有可能与苯胺具有 相关(选填编号)。苯胺可以由苯经过两步反应生成,写出第一步反应的化学方程式 、第二步反应的类型为 。
)是最简单的芳香胺,暴露于空气中变为棕色,该变化最有可能与苯胺具有 相关(选填编号)。苯胺可以由苯经过两步反应生成,写出第一步反应的化学方程式 、第二步反应的类型为 。
 )及其衍生物冬青油(结构简式:
)及其衍生物冬青油(结构简式: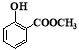 )和阿司匹林(结构简式:
)和阿司匹林(结构简式: )都是常用的药物。
)都是常用的药物。




