题目内容
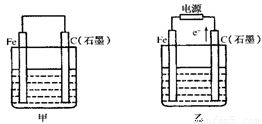
(9分)如图甲、乙是电化学实验装置。
(1)若甲、乙两烧杯中均盛有NaCl溶液。
①甲中石墨棒上的电极反应式为 ;
②乙中总反应的离子方程式为 ;
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5:1,且生成两种酸,该反应的化学方程式为:
。
(2)若甲、乙两烧杯中均盛有CuSO4溶液。
①甲中铁棒上的电极反应式为 。
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25 ℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入 (填写物质的化学式) g。
(1)①O2+2H2O+4e-===4OH-(2分) ②2Cl-+2H2O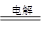 2OH-+H2↑+Cl2↑(2分)
2OH-+H2↑+Cl2↑(2分)
③5Cl2+I2+6H2O===10HCl+2HIO3(2分) (2)①Fe-2e-===Fe2+(1分)
②CuO(或CuCO3) (1分) 0.8(或1.24) (1分)
解析

练习册系列答案
相关题目