题目内容
8.据某科学杂志报道,国外发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60结构.下列叙述不正确的是( )| A. | 该物质的熔点不会很高、硬度不会很大 | |
| B. | 该物质形成的晶体属于分子晶体 | |
| C. | 该物质分子中Si60被包裹在C60里面 | |
| D. | 该物质的相对分子质量为2400 |
分析 A、根据分子晶体的熔点低、硬度小分析;
B、由分子式及信息可知该物质为分子晶体;
C、根据硅的原子半径比碳大;
D、根据分子式确定该物质的相对分子质量.
解答 解:A、由分子式及信息可知该物质为分子晶体,分子晶体的熔点低、硬度小,故A正确;
B、由题目中的信息可知是一种新的球形分子,它的分子式为C60Si60,所以该物质有分子存在,属于分子晶体,故B正确;
C、硅的原子半径比碳大,所以硅化合物Si60C60,外层球壳为Si60,内层球壳为C60,故C错误.
D、它的分子式为C60Si60,所以该物质的相对分子质量=(12+28)×60=2400,故D正确;
故选C.
点评 本题考查了晶体的物理性质、分子晶体的判断等知识点,难度不大,注意根据晶体的构成微粒来判断晶体类型.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
18.“化学,我们的生活,我们的未来”曾经是2011年“国际化学年”的主题.你认为下列行为中,不符合这一主题的是( )
| A. | 控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源 | |
| B. | 大量使用化肥和农药,以提高农作物产量 | |
| C. | 开发太阳能、水能、风能等新能源、减少使用煤、石油等化石燃料 | |
| D. | 实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle) |
19.下列有关反应速率的说法正确的是( )
| A. | 用铁片和稀硫酸反应制氢气时,改用98%的硫酸可以加快反应速率 | |
| B. | 100 mL 2 mol•L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| C. | SO2的催化氧化反应是一个放热的反应,所以升高温度,反应速率变慢 | |
| D. | 汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率变慢 |
16.MCFC型燃料电池可同时供应电和水蒸气,其工作温度为600℃~700℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2+O2=2H2O,则下列有关该电池的说法正确的是( )
| A. | 随着反应的进行,CO32-在不断消耗 | |
| B. | 该电池的正极的反应式为:4OH-+4e-=O2+2H2O | |
| C. | 放电时CO32-向正极移动 | |
| D. | 该电池负极的反应为:H2+CO32--2e-=H2O+CO2 |
3.X、Y都是短周期元素,X原子最外层只有一个电子,Y元素的最高正价与最低负价的代数和为6,X和Y两元素形成的化合物为R,下列叙述正确的是( )
| A. | R一定是气态 | |
| B. | R一定是离子化合物 | |
| C. | R一定是共价化合物 | |
| D. | R可能是离子化合物,也可能是共价化合物 |
13.下列实验方案能够达到目的是( )
| A. | 将溴乙烷与NaOH溶液混合后振荡、静置,直接向反应后的混合物中滴加AgNO3溶液,检验Br-的存在 | |
| B. | 将淀粉与稀H2SO4混合后加热,3min~4min后,直接向反应后的混合物中加入银氨溶液,检验葡萄糖的存在(已知淀粉在酸性条件下能水解成葡萄糖,葡萄糖含醛基) | |
| C. | 向试管中加入5mL溴水、2mL苯和0.5g铁粉,充分振荡后静置,观察试管底部生成的褐色油状液体 | |
| D. | 在试管中加入约2mL饱和溴水,然后滴入2滴~3滴苯酚稀溶液,观察苯酚与溴反应生成的白色沉淀 |
20.除去苯中含有的少量苯酚杂质常用的方法是( )
| A. | 加水振荡后用分液漏斗分离 | B. | 加溴水振荡后过滤 | ||
| C. | 加四氯化碳振荡后用分液漏斗分离 | D. | 加NaOH溶液振荡后用分液漏斗分离 |
17.23Na与23Na+比较,相同的是( )
| A. | 微粒半径 | B. | 化学性质 | C. | 最外层电子数 | D. | 中子数 |
18.下列电子式正确的是( )
| A. | H2O2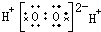 | B. | CCl4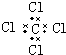 | C. | MgCl2 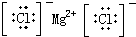 | D. | NaOH 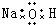 |