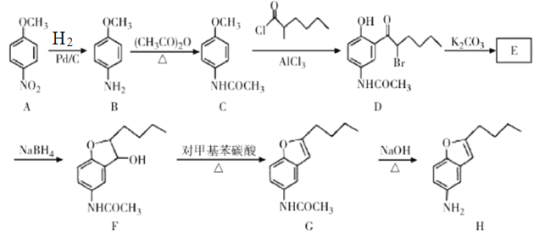
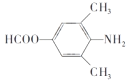
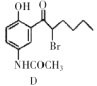
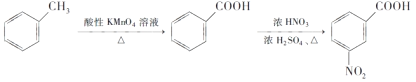
��Ŀ����
����Ŀ������˵��������ǣ� ��
A.�ö��Ե缫��� Na2SO4��Һ���� 2 mol����ת��ʱ,�ɼ��� 18 g ˮ�ָ�
B.�ö��Ե缫��� CuSO4��Һ��������1 mol Cu(OH)2�ָ����ǰŨ��ʱ����·��ת����4mol e��
C.��Mg��Al��������NaOH��Һ�����ԭ��أ�Mg��������Al������
D.Ҫ��ʵ�� Cu��H2SO4(ϡ) �T CuSO4��H2���ķ�Ӧ�����ڵ����н��У��� Cu Ϊ����
���𰸡�C
��������
A. �ö��Ե缫���Na2SO4��Һ�������������ӵķŵ�˳��Ϊ��OH>SO42����ŵ��ΪOH�������������ӵķŵ�˳��Ϊ��H+>Na+����ŵ��ΪH+����ʵ��Ϊ���ˮ��2H2O![]() 2H2��+O2������2mol����ת��ʱ��������1molˮ����ɼ���18gˮ�ָ���A����ȷ��
2H2��+O2������2mol����ת��ʱ��������1molˮ����ɼ���18gˮ�ָ���A����ȷ��
B. �ö��Ե缫���CuSO4��Һʱ���ȷ�����Ӧ2H2O+2CuSO4![]() 2Cu+O2��+2H2SO4����ʱ��Һ�൱������CuO������������Һ�ɼ�����⣬������Ӧ2H2O
2Cu+O2��+2H2SO4����ʱ��Һ�൱������CuO������������Һ�ɼ�����⣬������Ӧ2H2O![]() 2H2��+O2����������1 mol Cu(OH)2�ָ����ǰŨ�ȣ�Cu(OH)2������Ͽɿ���CuOH2O������������ʲô����ʲô����ԭ��֪������������������ͭ��ˮ��������������������ͭ������1molͭת�Ƶ���2mol�����1molˮ����1mol����������1mol����ת�Ƶ���2mol�����Ե������й�ת�Ƶ�����Ϊ4mol��B����ȷ��
2H2��+O2����������1 mol Cu(OH)2�ָ����ǰŨ�ȣ�Cu(OH)2������Ͽɿ���CuOH2O������������ʲô����ʲô����ԭ��֪������������������ͭ��ˮ��������������������ͭ������1molͭת�Ƶ���2mol�����1molˮ����1mol����������1mol����ת�Ƶ���2mol�����Ե������й�ת�Ƶ�����Ϊ4mol��B����ȷ��
C. Mg��NaOH��Һ����Ӧ��Al��NaOH��Һ�ܷ�Ӧ����Ӧ����ʽΪ2Al+2NaOH+2H2O=2NaAlO2+3H2�������Al��������C�����
D. Ҫʵ��Cu+H2SO4(ϡ)�TCuSO4+H2���ķ�Ӧ���÷�Ӧ�����Է����У����ڵ����н��У��ɷ��̿�֪��Cuʧȥ���ӷ���������Ӧ����Ϊ������D����ȷ��
��ѡC��

 Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�����Ŀ�������������Ǵ�����Ⱦ��֮һ���û���̿��һ����̼��ԭ��������ɷ�ֹ������Ⱦ���ش��������⣺
��֪��2C(s)+O2(g)=2CO(g) ��H=��221kJ��mol��1
C(s)+O2(g)=CO2(g) ��H=��393.5kJ��mol��1
N2(g)+O2(g)=2NO(g) ��H=+181kJ��mol-1
(1)��ij��Ӧ��ƽ�ⳣ������ʽΪK=![]() ����д���˷�Ӧ���Ȼ�ѧ����ʽ��_____�����д�ʩ�ܹ�����˷�Ӧ��NO��ת���ʵ���(����ĸ����)______��
����д���˷�Ӧ���Ȼ�ѧ����ʽ��_____�����д�ʩ�ܹ�����˷�Ӧ��NO��ת���ʵ���(����ĸ����)______��
A����������ѹǿB�������¶�C��ʹ�����ʴ���D������CO��Ũ��
(2)���ݻ�Ϊ2L���ܱ������м������̿(����)��NO��������ӦC(s)+2NO(g)![]() N2(g)+CO2(g)��NO��N2�����ʵ����仯���±���ʾ��
N2(g)+CO2(g)��NO��N2�����ʵ����仯���±���ʾ��
���ʵ���/mol | T1/�� | T2/�� | |||||
0 | 5min | 10min | 15min | 20min | 25min | 30min | |
NO | 2.0 | 1.16 | 0.80 | 0.80 | 0.50 | 0.40 | 0.40 |
N2 | 0 | 0.42 | 0.60 | 0.60 | 0.75 | 0.80 | 0.80 |
��05min�ڣ���CO2��ʾ�ĸ÷�Ӧ����v(CO2)=_______���������µ�ƽ�ⳣ��K=_____��
����15min���¶ȵ�����T2�����ݱ仯���ϱ���ʾ����T1____T2(����>������<������=��)��
����30minʱ������T2���䣬����������ټ�������ַ�Ӧ������2mol�����ʱ��Ӧ_____�ƶ�(����������������������������)�����մ�ƽ��ʱNO��ת����a=____________��
(3)��ҵ�Ͽ����ð�ˮ��ȥ��ӦC(s)+2NO(g)![]() N2(g)+CO2(g)�в�����CO2���õ�NH4HCO3��Һ����ӦNH4��+HCO3-+H2O
N2(g)+CO2(g)�в�����CO2���õ�NH4HCO3��Һ����ӦNH4��+HCO3-+H2O![]() NH3��H2O+H2CO3��ƽ�ⳣ��K=_____��(��֪������NH3��H2O�ĵ���ƽ�ⳣ��Kb=2��10-5��H2CO3�ĵ���ƽ�ⳣ��Ka1=4��10-7��Ka2=4��10-11)
NH3��H2O+H2CO3��ƽ�ⳣ��K=_____��(��֪������NH3��H2O�ĵ���ƽ�ⳣ��Kb=2��10-5��H2CO3�ĵ���ƽ�ⳣ��Ka1=4��10-7��Ka2=4��10-11)
����Ŀ������ˮ��ɽ���ǽ�ɽ��ɽ��������о�NOx��SO2�ȴ�����Ⱦ������ƴ���������Ҫ���塣
(1)SO2���ŷ���Ҫ������ú��ȼ�գ���ҵ�ϳ��ð�ˮ���շ�����β���е�SO2����֪���չ�������ط�Ӧ���Ȼ�ѧ����ʽ���£�
��SO2(g)+NH3��H2O(aq)==NH4HSO3(aq) ��H1=akJ��mol��1��
��NH3��H2O(aq)+NH4HSO3(aq)==(NH4)2SO3(ag)+H2O(l) ��H2=bkJ��mol��1��
��2(NH4)2SO3(aq)+O2(g)==2(NH4)2SO4(aq) ��H3=ckJ��mol��1��
��Ӧ2SO2(g)+4NH3��H2O(aq)+O2(g)==2(NH4)2SO4(aq)+2H2O(1)�ġ�H=___________kJ��mol��1��
(2)ȼú���糧�����÷�Ӧ2CaCO3(s)+2SO2(g)+O2(g)===2CaSO4(s)+2CO2(g)
��H=��681.8kJ��mol��1��ú����������������SO2���ŷš����ڸ÷�Ӧ����T��ʱ��������������÷�Ӧ�ڲ�ͬʱ����ϸ����ʵ�Ũ�����£�
0 | 10 | 20 | 30 | 40 | 50 | |
O2 | 1.00 | 0.79 | 0.60 | 0.60 | 0.64 | 0.64 |
CO2 | 0 | 0.42 | 0.80 | 0.80 | 0.88 | 0.88 |
��0~10min�ڣ�ƽ����Ӧ����v(O2)___________mol��L��1��min��1���������¶ȣ��÷�Ӧ��ƽ�ⳣ��K___________(��������������С������������)��
��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⡣�����ϱ��е������жϣ��ı������������___________(����ĸ)��
A����һ�����ķ�״̼��� Bͨ��һ������O2
C�ʵ���С��������� D������ʵĴ���
(3) NOx���ŷ���Ҫ����������β���������÷�Ӧ
C(s)+2NO(g)![]() N2(g)+CO2(g) ��H=��34.0kJ��mol��1���û���̿��NO������������֪���ܱ������м���������C��һ������NO���壬���ֺ�ѹ���NO��ת�������¶ȵı仯��ͼ��ʾ��
N2(g)+CO2(g) ��H=��34.0kJ��mol��1���û���̿��NO������������֪���ܱ������м���������C��һ������NO���壬���ֺ�ѹ���NO��ת�������¶ȵı仯��ͼ��ʾ��

��ͼ��֪��1050Kǰ��Ӧ��NO��ת�������¶����{��������ԭ��Ϊ____________________����1100Kʱ��CO2���������Ϊ___________��
(4)��ij���ʵ�ƽ���ѹ���������ʵ���Ũ��Ҳ���Ա�ʾ��ѧƽ�ⳣ��(����Kp)����1050K��1.1��106Paʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Kp=___________[��֪�������ѹ(P��)=������ѹ(Pa)���������]��
(5)Ϊ��������β���е��к�����Դ�������Ⱦ�����������װβ������װ�á��ھ���װ����CO��NO������Ӧ2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ��H=��746.8k��mol��1����������N2��CO2��ʵ���ã�v��=k����c2(NO)��c2(CO)��v��=k����c(N2) ��c2(CO2)(k����k��Ϊ���ʳ�����ֻ���¶��й�)��
N2(g)+2CO2(g) ��H=��746.8k��mol��1����������N2��CO2��ʵ���ã�v��=k����c2(NO)��c2(CO)��v��=k����c(N2) ��c2(CO2)(k����k��Ϊ���ʳ�����ֻ���¶��й�)��
�ٴﵽƽ��������¶ȣ�k������ı���___________(����>����<������=��)k������ı�����
������1L���ܱ������г���1 molCO��1 molNO����һ���¶��´ﵽƽ��ʱ��CO��ת����Ϊ40%����![]() =___________��
=___________��