题目内容
15.NA为阿伏伽德罗常数,下列说法正确的是( )| A. | 16g CH4与18g NH4+所含的质子数为10NA | |
| B. | 将15.6g Na2O2投入到足量水中,反应后溶液中的氧原子数为0.4NA | |
| C. | 在1L 0.1mol•L-1的碳酸钠溶液中,阴离子总数一定大于0.1NA | |
| D. | 2mol NO和1mol O2混合,所得气体的分子数为2NA |
分析 A.甲烷分子中含有10个质子,而铵根离子中含有11个质子;
B.将过氧化钠投入水中,水分子中也含有氧原子;
C.碳酸根离子部分水解,导致阴离子数目增多;
D.二氧化氮与四氧化二氮之间存在转化平衡.
解答 解:A.16g甲烷和18g 铵根离子的物质的量都是1mol,1mol甲烷分子中含有10mol质子,而1mol铵根离子中含有11mol质子,二者含有的质子数不同,故A错误;
B.由于水分子中含有氧原子,则无法计算反应后溶液中含有的氧原子数目,故B错误;
C.1L 0.1mol•L-1的碳酸钠溶液中含有0.1mol碳酸钠,由于碳酸根离子水解生成碳酸氢根离子和氢氧根离子,导致溶液中阴离子数目增多,所以阴离子总数一定大于0.1NA,故C正确;
D.2mol NO和1mol O2混合,二者恰好反应生成2mol二氧化氮,由于部分二氧化氮转化成四氧化二氮,则反应后气体分子数小于2NA,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的综合应用,题目难度中等,明确物质的量与阿伏伽德罗常数、摩尔质量、物质的量浓度等之间的关系为解答关键,D为易错点,注意二氧化氮与四氧化二氮之间存在转化平衡.

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
5.下列括号中的物质是除去杂质所需的药品,其中错误的是( )
| A. | NaCl溶液中有杂质Na2SO4(氯化钡) | B. | FeS04溶液中有杂质CuSO4(铁粉) | ||
| C. | 生石灰中混有少量石灰石(盐酸) | D. | BaCl2溶液中有少量MgCl2(氢氧化钡) |
6.在含等物质的量浓度的Fe3+、NH4+、H+、Al3+溶液中,逐滴滴加氢氧化钠溶液,生成物依次产生的顺序是( )
| A. | Fe(OH)3、H2O、Al(OH)3、NH3•H2O、NaAlO2 | B. | Al(OH)3、NH3、H2O、Fe(OH)3、NaAlO2、H2O | ||
| C. | H2O、Fe(OH)3、Al(OH)3、NH3•H2O、NaAlO2 | D. | H2O、Fe(OH)3、Al(OH)3、NaAlO2、NH3•H2O |
3.两种金属混合粉末15g,与足量的盐酸反应时生成11.2L氢气(标准状况),符合上述情况的金属混合物的是( )
| A. | Mg和Al | B. | Mg和Ag | C. | Na和Zn | D. | Fe和Zn |
10.下列有关电解质的说法中正确的是( )
| A. | 液态HCl不导电,因此HCl是非电解质 | |
| B. | Na2O熔融态时能导电,所以Na2O是电解质 | |
| C. | 液态的铜导电性很好,所以铜是电解质 | |
| D. | CO2水溶液能导电,所以CO2是电解质. |
20.某强碱性溶液中含有的离子是K+、NH4+、A13+、AlO2-、CO32-、SiO32-、Cl-中的某几种,现进行如下实验:
①取少量的溶液用硝酸酸化后,该溶液无沉淀生成;
②另取一定量原溶液,逐滴加入盐酸至过量,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变,后产生一种气体,最后沉淀逐渐减少至消失.
③另取一定量的原溶液中加入5mL0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g.
下列说法中正确的是( )
①取少量的溶液用硝酸酸化后,该溶液无沉淀生成;
②另取一定量原溶液,逐滴加入盐酸至过量,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变,后产生一种气体,最后沉淀逐渐减少至消失.
③另取一定量的原溶液中加入5mL0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g.
下列说法中正确的是( )
| A. | 该溶液中一定不含K+、NH4+、A13+、SiO32- | |
| B. | 该溶液中一定含有A13+、CO32-、Cl- | |
| C. | 该溶液中可能含有Cl- | |
| D. | 该溶液中一定含有K+、AlO2-、CO32-、Cl- |
17.下列元素在自然界中只以化合态存在的( )
| A. | O | B. | Cl | C. | N | D. | Fe |
18.下列关于如图所示转化关系(X代表卤素)的说法错误的是( )
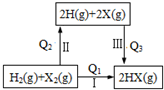

| A. | Q3>0 | B. | Q1=Q2+Q3 | ||
| C. | 按Cl、Br、I的顺序,Q2依次增大 | D. | Q1越大,HX越稳定 |