题目内容
10.0.5mol Na2SO4•10H2O中所含的Na+、SO42-的物质的量各是多少?所含结晶水数目是多少?分析 钠离子物质的量等于Na2SO4•10H2O物质的量的2倍,硫酸根物质的量等于Na2SO4•10H2O的物质的量,结晶水的物质的量为Na2SO4•10H2O物质的量的10倍,根据N=nNA计算结晶水数目.
解答 解:n(Na+)=2n(Na2SO4•10H2O)=0.5mol×2=1mol,n(SO42-)=n(Na2SO4•10H2O)=0.5mol,结晶水的物质的量为0.5mol×10=5mol,所含结晶水数目是5mol×6.02×1023mol-1=3.01×1024,
答:0.5mol Na2SO4•10H2O中所含的Na+、SO42-的物质的量各是1mol、0.5mol,所含结晶水数目是3.01×1024.
点评 本题考查物质的量有关计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图,下列说法不正确的是( )
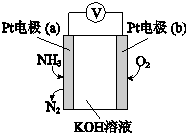

| A. | O2在电极b上发生还原反应 | |
| B. | 溶液中OH-向电极b移动 | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:3 | |
| D. | 负极的电极反应式为:2NH3-6e-+6OH-═N2+6H2O |
1.下列叙述中正确的是( )
| A. | 第三周期元素的离子半径从左到右依次减小 | |
| B. | HCl、PCl5、N2、CO2分子中所有原子都满足最外层8电子的结构 | |
| C. | 晶体内可以不存在化学键,也可以同时存在离子键和共价键 | |
| D. | 若某离子化合物X2Y3中X3+和Y2-的电子层结构相同,则X、Y两元素的原子序数之差可能是5、15或29 |
5.取一定质量的Cu2O与CuO的固体混合物.将其分成两等份.向其中一份通入足量的氢气,充分反应后固体质量为25.6g,另一份加入500mL稀硝酸中,固体恰好完全溶解并产生标准状态下的NO气体4.48L.已知Cu2O+2H+═Cu+Cu2++H2O.则稀硝酸的浓度为( )
| A. | 2mol•L-1 | B. | 1.6mol•L-1 | C. | 0.8mol•L-1 | D. | 0.4mol•L-1 |
15.将pH=3的CH3COOH与pH=11的NaOH溶液等体积混合后,所得的混合溶液中,下列关系式正确的是( )
| A. | c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | B. | c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | ||
| C. | c(CH3COO-)>c(H+)>c(Na+)>c(OH-) | D. | c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
 根据右图回答下列问题:
根据右图回答下列问题: