题目内容
14.在人类已知的化合物中,数量最多的是( )| A. | 过渡元素形成的化合物 | B. | 第ⅢA族元素形成的化合物 | ||
| C. | 第ⅣA族元素形成的化合物 | D. | 第ⅦA族元素形成的化合物 |
分析 根据有机物化合物在生活、生产中的应用及有机物的种类来分析,有机物种类最多,有机物的基本元素为C元素,据此进行解答.
解答 解:A.过渡元素的化合物,为金属化合物,化合物中品种有限,故A错误;
B.第ⅢA族元素的化合物主要有氧化物、氢氧化物、盐等,化合物中品种有限,故B错误;
C.第ⅣA族元素的化合物为碳族元素,主要为氧化物、酸、盐及某些氢化物,形成的有机化合物已超过3000万种,化合物品种最多,故C正确;
D.第ⅤⅡA族元素的化合物为卤族元素,主要为氧化物、酸、盐及某些氢化物,化合物中品种有限,故C错误;
故选C.
点评 本题考查元素周期表结构及应用,题目难度不大,明确原子结构与元素周期表结构的关系为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
4.下列有关化学键的说法正确的是( )
| A. | 离子化合物中一定含有离子键,共价化合物中可能含有离子键 | |
| B. | 共价化合物中一定含有共价键,离子化合物中可能含有共价键 | |
| C. | 由非金属元素形成的化合物中一定只含共价键 | |
| D. | 含有金属元素的化合物中一定含有离子键 |
5.C60是60个碳原子形成的封闭笼状分子,形似足球,它与石墨互为( )
| A. | 同分异构体 | B. | 同素异形体 | C. | 同位素 | D. | 同一物质 |
2.固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列有关说法不正确的是( )
| A. | 1 mol NH5中含有5 NA个N-H键(NA表示阿伏加德罗常数) | |
| B. | NH5中既有共价键又有离子键 | |
| C. | NH5与NH4Cl 中阳离子的电子式相同 | |
| D. | 它与水反应的离子方程式为:NH4++H-+H2O═NH3•H2O+H2↑ |
9.常温下,醋酸和氨水的电离平衡常数均为1.8×10-5.向10mL浓度为0.1mol•L-1的NH3•H2O溶液中滴加相同浓度的CH3COOH(温度变化忽略不计),在滴加过程中( )
| A. | c(NH4+)与c(NH3•H2O)之和始终保持不变 | |
| B. | 水的电离程度始终增大 | |
| C. | $\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$始终减小 | |
| D. | 当加入CH3COOH的体积为10mL时,溶液pH>7 |
19.气体A、B通式分别为CnH2n+2和CnH2n,若用催化剂使250mL混合气体加氢,在相同条件下需要H2100mL,则原混合气体中A、B两体积之比为( )
| A. | 1:2 | B. | 1:3 | C. | 1:4 | D. | 3:2 |
6.已知一定温度时:N2(g)+3H2(g)?2NH3(g).当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入0.1mol N2和0.3mol H2,达到平衡时放出热量为Q.则下列关系式中正确的是( )
| A. | Q=9.2 kJ | B. | Q>9.2 kJ | C. | Q<9.2 kJ | D. | Q=18.4kJ |
3.图是某有机物分子的比例模型,则该物质不具有的性质是( )


| A. | 与钠反应 | B. | 发生氧化反应 | C. | 发生酯化反应 | D. | 使紫色石蕊变红 |



 ;
;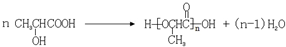 ;
;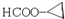 .
.