题目内容
6.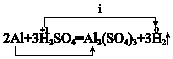 有四种物质:①氧化铝 ②稀硫酸 ③碳酸氢钠 ④氢氧化钠
有四种物质:①氧化铝 ②稀硫酸 ③碳酸氢钠 ④氢氧化钠(1)属于盐的物质是③(填序号,下同).
(2)既能与强酸反应,又能与强碱反应的物质是①③.
(3)分析铝与稀硫酸反应,i表示的内容为b.
a.得到e-×6,化合价升高,被还原b.得到e-×6,化合价降低,被还原c.失去e-×6,化合价升高,被氧化.
分析 (1)碳酸氢钠是盐;
(2)氧化铝是两性氧化物,既能与强酸反应,又能与强碱反应的物质,碳酸氢钠是多元弱酸的酸式盐,是既能与强酸反应,又能与强碱反应的物质;
(3)氢离子得到e-×6,化合价降低,被还原,由此分析解答.
解答 解:(1)碳酸氢钠是盐,所以选:③,故答案为:③;
(2)氧化铝是两性氧化物,既能与强酸反应,又能与强碱反应的物质,碳酸氢钠是多元弱酸的酸式盐,是既能与强酸反应,又能与强碱反应的物质,故答案为:①③;
(3)氢离子得到e-×6,化合价降低,被还原,所以符合条件的是b,故选:b.
点评 本题考查两性氧化物和氧化还原反应的知识,注意具有两性和与酸、碱反应的区别,(2)为解答的易错点,把握碳酸氢钠可与某些酸碱反应即可解答.

练习册系列答案
相关题目
16.根据元素周期律,由下列事实进行归纳推测,推测不合理的是( )
| 选项 | 事实 | 推测 |
| A. | Na与冷水反应剧烈,K与冷水反应更剧烈 | Li与冷水反应缓慢 |
| B. | 20Ca(OH)2碱性强于12Mg(OH)2 | 38Sr(OH)2碱性强于20Ca(OH)2 |
| C. | Si是半导体材料,同主族的Ge也是半导体材料 | 第ⅣA元素形成的单质都是半导体材料 |
| D. | F2与H2在暗处剧烈化合,Cl2与H2光照或点燃时反应 | Br2与H2反应需要加热到一定温度 |
| A. | A | B. | B | C. | C | D. | D |
17.将一小块金属钠放在坩埚里加热,实验现象描述正确的是( )
①钠在燃烧之前先熔化 ②钠燃烧的火焰呈紫色
③钠燃烧后得到白色固体 ④钠燃烧的火焰呈黄色
⑤钠燃烧后生成物为淡黄色固体.
①钠在燃烧之前先熔化 ②钠燃烧的火焰呈紫色
③钠燃烧后得到白色固体 ④钠燃烧的火焰呈黄色
⑤钠燃烧后生成物为淡黄色固体.
| A. | ①④⑤ | B. | 只有⑤ | C. | 只有① | D. | ②③ |
14.当光束通过下列分散系时,可观察到丁达尔效应的是( )
| A. | 硫酸铜溶液 | B. | 氢氧化铁胶体 | C. | 蔗糖溶液 | D. | 氯化钠溶液 |
1.下列操作不能达到预期目的是( )
| A. | 用蒸馏法将自来水制成蒸馏水 | B. | 用酒精萃取碘水中的碘 | ||
| C. | 用过滤法除去食盐水中的泥沙 | D. | 用淘洗的方法从沙里淘金 |
11.下列有关化学用语表示正确的是( )
| A. | 氨气分子的电子式: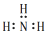 | B. | Mg2+结构示意图  | ||
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U互为同位素 | D. | 乙醇的分子式C2H5OH |
18.最近全面通车的沪昆高速铁路是国家重要的交通线路,在工程建设中用量最大的硅酸盐材料是( )
| A. | 钢筋 | B. | 水泥 | C. | 玻璃 | D. | 陶瓷 |
13.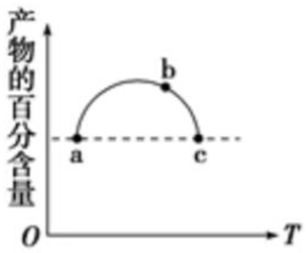 在恒容容器中充入一定量的SO2和Cl2,发生反应SO2(g)+Cl2(g)?SO2Cl2(g),测得体系中产物的百分含量与反应温度的变化如图所示,下列说法正确的是( )
在恒容容器中充入一定量的SO2和Cl2,发生反应SO2(g)+Cl2(g)?SO2Cl2(g),测得体系中产物的百分含量与反应温度的变化如图所示,下列说法正确的是( )
 在恒容容器中充入一定量的SO2和Cl2,发生反应SO2(g)+Cl2(g)?SO2Cl2(g),测得体系中产物的百分含量与反应温度的变化如图所示,下列说法正确的是( )
在恒容容器中充入一定量的SO2和Cl2,发生反应SO2(g)+Cl2(g)?SO2Cl2(g),测得体系中产物的百分含量与反应温度的变化如图所示,下列说法正确的是( )| A. | a、b、c三点均为平衡点 | |
| B. | a、c两点的反应速率相同 | |
| C. | b点对应温度的平衡常数大于c点对应温度的平衡常数 | |
| D. | a、c两点体系的压强相同 |
14.下列离子方程式正确的是( )
| A. | 硫化钠溶液显碱性:S2-+H2O═HS-+OH- | |
| B. | 硫酸铜溶液呈酸性:Cu2++2H2O?Cu(OH)2↓+2H+ | |
| C. | 氯化铝溶液与碳酸钠溶液混合:Al3++CO32-═Al(OH)3↓+H2↑ | |
| D. | 在饱和氯化铵溶液中撒入镁粉后微热:2NH4++Mg═Mg2++2NH3↑+H2↑ |