题目内容
【题目】Al、Fe、Cu都是重要的金属元素,下列说法正确的是
A.三者对应的氧化物均为碱性氧化物
B.三者的单质放置在空气中均只生成氧化物
C.Fe2O3 与Fe3O4互为同素异形体
D.常温下三者加入浓硫酸中均无明显现象
【答案】D
【解析】
试题分析:A、铝对应的氧化物Al2O3是两性氧化物,故A错误;B、Fe还可以形成复杂的氢氧化物,Cu可以形成碱式碳酸铜等,故B错误;C.Fe2O3 与Fe3O4都是Fe的氧化物,不是同素异形体,故C错误;D.常温下Al、F加入浓硫酸中会发生钝化现象,而Cu在浓硫酸中,不具备反应条件,因此不会发生反应,故D正确;故选D。

【题目】(Ⅰ)俄美科学家联合小组宣布合成出114号元素(Fl)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中位于第___________周期,___________族,属于金属元素还是非金属元素? ___________。
(2)该原子核内中子数为___________;
(3)如果该元素存在最高价氧化物对应的水化物,请写出其化学式___________;
(Ⅱ)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
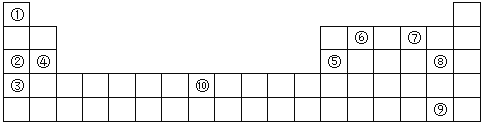
(1)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是___________(填化学式)。
(2)10种元素中,原子半径最小的是___________(填序号)。
(3)元素⑦的氢化物与⑧的单质反应的离子方程式为___________;
(4)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为___________;
(5)元素⑩的原子序数为___________,其单质与⑦的氢化物高温下反应的化学方程式为___________;
(6)单质⑨易溶于⑥与⑧形成的化合物中,所得溶液颜色为___________色。
(Ⅲ)判断以下叙述正确的是___________
部分短周期元素的原子半径及主要化合价
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物一定具有两性
D.氢化物的沸点为HnT>HnR
E.T与R形成的TR2、TR3均为共价化合物
F. Q与M的单质均能与盐酸、NaOH溶液反应放出氢气