题目内容
将CoCl2溶解于盐酸中可以形成CoCl42-,在溶液中存在下面的化学平衡:Co2+(aq)+4Cl-(aq)?CoCl42-(aq)△H>0 下列说法正确的是( )
分析:A.升高温度,正、逆反应速率都增大;
B.化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写判断;
C.Co2+为红色,CoCl42-是蓝色,该反应正反应是吸热反应,升高温度平衡向正反应移动;
D.通入少量HCl气体,平衡正向移动,Co2+浓度都减小,移动的结果是降低氯离子浓度增大,不可能消除Cl-浓度增大.
B.化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写判断;
C.Co2+为红色,CoCl42-是蓝色,该反应正反应是吸热反应,升高温度平衡向正反应移动;
D.通入少量HCl气体,平衡正向移动,Co2+浓度都减小,移动的结果是降低氯离子浓度增大,不可能消除Cl-浓度增大.
解答:解:A.升高温度,正、逆反应速率都增大,但正反应速率增大更多,故A错误;
B.Co2+(aq)+4Cl-(aq)?CoCl42-(aq)的化学平衡常数k=
,故B正确;
C.Co2+为红色,CoCl42-是蓝色,该反应正反应是吸热反应,升高温度平衡向正反应移动,溶液呈蓝色,故C错误;
D.通入少量HCl气体,平衡正向移动,Co2+浓度都减小,Cl-浓度增大,故D错误;
故选B.
B.Co2+(aq)+4Cl-(aq)?CoCl42-(aq)的化学平衡常数k=
| c(CoCl42-) |
| c(Co2+)?c4(Cl-) |
C.Co2+为红色,CoCl42-是蓝色,该反应正反应是吸热反应,升高温度平衡向正反应移动,溶液呈蓝色,故C错误;
D.通入少量HCl气体,平衡正向移动,Co2+浓度都减小,Cl-浓度增大,故D错误;
故选B.
点评:本题考查温度对反应速率的影响、化学平衡的影响因素、化学平衡常数等,难度中等,D选项可以借助平衡常数进行理解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将CoCl2溶解于盐酸中可以形成CoCl42—,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq) CoCl42—(aq) ΔH>0
CoCl42—(aq) ΔH>0
粉 红色 蓝色
红色 蓝色
下列说法正确的是
A.升高温度,正 反应速率增大,逆反应速率减小 反应速率增大,逆反应速率减小 |
B.该反应的平衡常数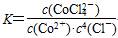 |
| C.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色 |
| D.增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小 |
 CoCl42—(aq) ΔH>0
CoCl42—(aq) ΔH>0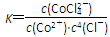
 CoCl(aq) ΔH>0
CoCl(aq) ΔH>0