题目内容
将CoCl2溶解于盐酸中可以形成CoCl42-,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq)?CoCl
(aq)△H>0
粉红色 蓝色
下列说法正确的是( )
Co2+(aq)+4Cl-(aq)?CoCl
2- 4 |
粉红色 蓝色
下列说法正确的是( )
分析:A、温度变化对反应速率的影响是升高温度正逆反应速率增大,只是增大程度不同;
B、依据平衡常数概念分析写出;
C、反应是吸热反应,温度升高平衡正向进行;
D、增大氯离子浓度,平衡正向进行,钴离子浓度减小,氯离子浓度增大;
B、依据平衡常数概念分析写出;
C、反应是吸热反应,温度升高平衡正向进行;
D、增大氯离子浓度,平衡正向进行,钴离子浓度减小,氯离子浓度增大;
解答:解:A、温度变化对反应速率的影响是升高温度正逆反应速率增大,只是增大程度不同,升高温度,正反应速率增大,逆反应速率增大;故A错误;
B、Co2+(aq)+4Cl-(aq)?CoCl
(aq)△H>0,依据平衡常数的概念得到,K=
,故B正确;
C、反应是吸热反应,温度升高平衡正向进行,将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为蓝色,故C错误;
D、增大Cl-浓度,平衡向正反应方向移动,Co2+、浓度都减小,Cl-浓度增大,故D错误;
故选B.
B、Co2+(aq)+4Cl-(aq)?CoCl
2- 4 |
| c(COCl42-) |
| c(Co2+)c4(Cl-) |
C、反应是吸热反应,温度升高平衡正向进行,将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为蓝色,故C错误;
D、增大Cl-浓度,平衡向正反应方向移动,Co2+、浓度都减小,Cl-浓度增大,故D错误;
故选B.
点评:本题考查了化学平衡的影响因素分析,平衡常数的计算应用,掌握基础和平衡移动原理是解题关键,题目难度中等.

练习册系列答案
相关题目
将CoCl2溶解于盐酸中可以形成CoCl42—,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq) CoCl42—(aq) ΔH>0
CoCl42—(aq) ΔH>0
粉 红色 蓝色
红色 蓝色
下列说法正确的是
A.升高温度,正 反应速率增大,逆反应速率减小 反应速率增大,逆反应速率减小 |
B.该反应的平衡常数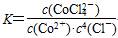 |
| C.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色 |
| D.增大Cl-浓度,平衡向正反应方向移动,Co2+、Cl-浓度都减小 |
 CoCl42—(aq) ΔH>0
CoCl42—(aq) ΔH>0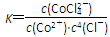
 CoCl(aq) ΔH>0
CoCl(aq) ΔH>0