题目内容
11.按要求完成下列问题:(1)甲基的电子式
 .
.(2)写出由甲苯制备TNT的化学反应方程式
 .
.(3)相对分子质量为72且只有一种一氯代物的烷烃的结构简式

(4)反式2一丁烯的结构简式

(5)与H2加成生成2,5一二甲基己烷的炔烃的系统命名2,5-二甲基-3-己炔
(6)
 的系统命名4-甲基-2-乙基-1-戊烯.
的系统命名4-甲基-2-乙基-1-戊烯.
分析 (1)甲基中C周围有7个电子;
(2)甲苯与浓硝酸、浓硫酸发生取代反应生成TNT;
(3)分子质量为72的烷烃,由CnH2n+2可知,14n+2=72,解得n=5,只有一种一氯代物,则只有一种H;
(4)反式2一丁烯中2个甲基在碳碳双键的两侧;
(5)与H2加成生成2,5一二甲基己烷的炔烃,碳链骨架不变,只有3、4号C上可存在三键;
(6)含碳碳双键的最长碳链有5个C,2号C上有乙基,4号C上有甲基.
解答 解:(1)甲基的电子式为 ,故答案为:
,故答案为: ;
;
(2)甲苯与浓硝酸、浓硫酸发生取代反应生成TNT,取代反应为 ,
,
故答案为: ;
;
(3)分子质量为72的烷烃,由CnH2n+2可知,14n+2=72,解得n=5,只有一种一氯代物,则只有一种H,则符合条件的烷烃为 ,
,
故答案为: ;
;
(4)反式2一丁烯中2个甲基在碳碳双键的两侧,其结构简式为 ,
,
故答案为: ;
;
(5)与H2加成生成2,5一二甲基己烷的炔烃,碳链骨架不变,只有3、4号C上可存在三键,则炔烃的名称为2,5-二甲基-3-己炔,
故答案为:2,5-二甲基-3-己炔;
(6)含碳碳双键的最长碳链有5个C,2号C上有乙基,4号C上有甲基,系统命名为4-甲基-2-乙基-1-戊烯,
故答案为:4-甲基-2-乙基-1-戊烯.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、结构及命名等为解答的关键,侧重分析与应用能力的考查,注意化学用语的使用,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
9.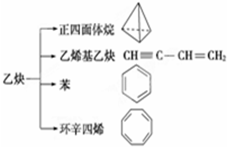 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )| A. | 正四面体烷的分子式为C4H4,其二氯代物有两种 | |
| B. | 苯为平面六边形结构,分子中存在C-C和C═C,能使酸性KMnO4溶液褪色 | |
| C. | 等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同 | |
| D. | 环辛四烯跟苯的结构很像,不能使溴水褪色 |
6.可以鉴别葡萄糖溶液的试剂是( )
| A. | 银氨溶液 | B. | 氢氧化铜固体 | C. | 石蕊试液 | D. | 碳酸钠溶液 |
3.有5种元素X、Y、Z、Q、T.X原子M层上有2个未成对电子且M层无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的P能级上只有一对成对电子;T原子的M电子层上p轨道半充满.下列叙述不正确的是( )
| A. | 元素Y和Q可形成化合物Y3Q4 | |
| B. | T和Z各有一种单质的空间构型为正四面体形,键角都是109°28? | |
| C. | X和Q结合生成的化合物可以形成离子化合物 | |
| D. | ZQ2是极性键构成的非极性分子 |
20.下列有关的离子方程式书写正确的是( )
| A. | NH4Cl溶液和浓的KOH溶液反应:NH4++OH-═NH3•H2O | |
| B. | 铜与稀硝酸反应:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 铜片插入硝酸银溶液中:Cu+Ag+═Ag+Cu2+ |
1.下列各组物质中,化学键全部为共价键的是( )
| A. | NH4Cl、CO2、HCl | B. | O2、KF、SO2 | C. | HCl、CH3COOH、CH4 | D. | Na2O2、N2、H2O |