题目内容
3.下列反应属于吸热反应的是( )①加热KClO3和MnO2的混合物制取O2②蜡烛的燃烧 ③将氢氧化钡晶体和氯化铵晶体的混合物放入水中 ④将生石灰倒入海水中 ⑤煅烧石灰石.
| A. | ①③⑤ | B. | ②③④ | C. | ②④ | D. | ①②③④⑤ |
分析 常见的放热反应有:所有的物质燃烧、所有金属与酸或与水、所有中和反应、绝大多数化合反应、铝热反应;
常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和CO2)、工业制水煤气、碳(一氧化碳、氢气)还原金属氧化物、某些复分解(如铵盐和强碱).
解答 解:①加热KClO3和MnO2的混合物制取O2时二氧化锰只做催化剂,此反应是KClO3的分解反应,故为吸热反应;
②所有的燃烧均为放热反应,故蜡烛的燃烧放热;
③铵盐和碱的反应为吸热反应,故将氢氧化钡晶体和氯化铵晶体的混合物放入水中反应吸热;
④将生石灰倒入海水中发生了CaO和水的化合反应,故为放热反应;
⑤煅烧石灰石发生了碳酸钙的分解反应,故为吸热反应.
故选A.
点评 本题考查化学反应中能量变化,题目难度不大,掌握常见的放热反应和吸热反应是解题的关键.

练习册系列答案
相关题目
11.下列曲线图与对应选项错误的是( )
| A. |  向1L浓度均为0.1mol/L的Ba(OH)2、NaAlO2混合溶液中逐滴加入0.1mol/l是H2SO4溶液 | |
| B. | 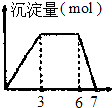 向含0.1mol/L的AlCl3和0.3mol/LNH4Cl的1L混合溶液中逐滴加入0.1mol/l是NaOH溶液 | |
| C. | 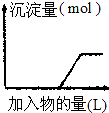 向烧碱溶液中逐滴加入明矾溶液 | |
| D. | 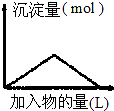 向Ba(OH)2溶液中逐渐通入二氧化碳气体 |
18.下列说法正确的是( )
| A. | P2O5可用于干燥Cl2和NH3 | |
| B. | 用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2 | |
| C. | 通过浓硫酸除去HCl中的H2O | |
| D. | 通过灼热的CuO除去H2中的CO |
15.下列烷烃中,能由相应的炔烃与 H2加成制得的是( )
| A. |  | B. |  | C. | 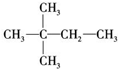 | D. | 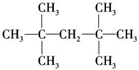 |
12.下列方法适合实验室制取氨气的是( )
| A. | N2和H2催化加热制取氨气 | B. | 加热NH4Cl制取氨气 | ||
| C. | 将浓氨水向氧化钙固体上滴加 | D. | 将NH4Cl溶液和NaOH溶液混合 |
2.氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
(1)BCl3的空间构型为;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生.
A. CsICl2═CsCl+ICl
B. CsICl2═CsI+Cl2
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是I.
(4)下列分子既不存在s-pσ键,也不存在p-pπ键的是D.
A. HCl B.HF C.CO2 D. SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3杂化,写出CN-的等电子体的分子式(写出1个)N2或CO.
(6)由H、N、O三种元素组成的常用作化肥,且水溶液显酸性化合物固态时属于离子晶体,假设其晶体的空间结构与氯化钠相似,且晶胞的棱长为acm,则该晶胞的密度为$\frac{320}{{N}_{A}•{a}^{3}}$g/cm3.
(1)BCl3的空间构型为;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生.
A. CsICl2═CsCl+ICl
B. CsICl2═CsI+Cl2
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是I.
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(KJ/mol) | 1681 | 1251 | 1140 | 1008 |
A. HCl B.HF C.CO2 D. SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中心氯原子的杂化轨道类型为sp3杂化,写出CN-的等电子体的分子式(写出1个)N2或CO.
(6)由H、N、O三种元素组成的常用作化肥,且水溶液显酸性化合物固态时属于离子晶体,假设其晶体的空间结构与氯化钠相似,且晶胞的棱长为acm,则该晶胞的密度为$\frac{320}{{N}_{A}•{a}^{3}}$g/cm3.
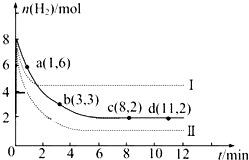 工业上“固定”和利用CO2能有效地减轻“温室”效应,可用CO2生产燃料甲醇:
工业上“固定”和利用CO2能有效地减轻“温室”效应,可用CO2生产燃料甲醇: