��Ŀ����
��12�֣�����ѧ�ḻ��ʣ����ڸ�����Ⱥã����������������������棬ͬ��������ɸ������ܵIJ���֡�K2Cr2O7��CrO3�����������ӡȾ�����ϡ���Ƶȹ�ҵ�У��ǹ�ҵ����ɸ���Ⱦ����Ҫԭ���ڱ���ġ������ҡ��¼��У�������Ϊ�ù�ҵƤ����½��ϻ���ƤЬ��Ϊԭ���ƳɵĹ�ҵ������ð���ʳ�������Ƴɽ��ң���ɽ����ڵĸ����س��ꡣ
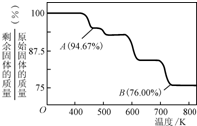
��1��CrO3�����ȶ��Խϲ����ʱ�ֽ⣬�������������¶ȵı仯��ͼ��ʾ�� 
��A ��ʱʣ�����ijɷ��� ���ѧʽ����
�ڴӿ�ʼ���ȵ� 750K ʱ�ܷ�Ӧ����ʽΪ ��
��2��Cr(��)��Ҫ��CrO42����Cr2O72����̬���ڣ������������¾��к�ǿ�������ԣ���������Һ�д�������ת����CrO42��(��ɫ)+2H+ Cr2O72��(��ɫ��+H2O��K=4.2��1014����Ҫʹ��Һ�ɻ�ɫ���ɫ����Ӧ��ȡ�Ĵ�ʩ�� ��
Cr2O72��(��ɫ��+H2O��K=4.2��1014����Ҫʹ��Һ�ɻ�ɫ���ɫ����Ӧ��ȡ�Ĵ�ʩ�� ��
| A����NaOH | B�������� | C�������� | D����AgNO3 |
�ٵ������� NaCl �������� ��
��д�������ĵ缫��Ӧʽ ��
��д��Fe2����Cr2O72��������Ӧ����Fe3����Cr3�������ӷ�Ӧ����ʽ ��
����֪�������Һ��c(Fe3��)=2.0��10��13 mol��L��1������Һ��c(Cr3��)Ϊ mol��L��1��
��1����Cr3O8����CrO2.67) ��2�֣� �� 4CrO32Cr2O3��3O2����2�֣�
��2��C ��2�֣� (3) ����ǿ��Һ�ĵ����� ��1�֣� ��Fe-2e��=Fe2+ ��1�֣�
��6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O ��2�֣���3.0��10��6 ��2�֣�
����

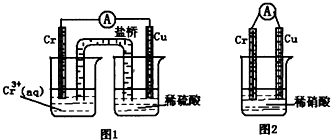
 �����������ж���������Σ���ܴ���˺�����ˮ������д��������ŷţ�
�����������ж���������Σ���ܴ���˺�����ˮ������д��������ŷţ�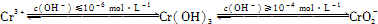
 ����ѧ�ḻ��ʣ����ڸ�����Ⱥã����������������������棬ͬ��������ɸ������ܵIJ���֣�CrO3���������ڵ�ƹ�ҵ�У�
����ѧ�ḻ��ʣ����ڸ�����Ⱥã����������������������棬ͬ��������ɸ������ܵIJ���֣�CrO3���������ڵ�ƹ�ҵ�У�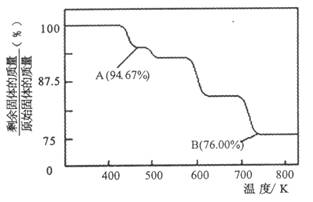

 Cr2O72������ɫ��+H2O
Cr2O72������ɫ��+H2O