题目内容
1.下列关于物质性质变化的比较不正确的是( )| A. | NaOH、Mg(OH)2、Al(OH)3的碱性逐渐增强 | B. | HClO4、HBrO4、HIO4的酸性逐渐减弱 | ||
| C. | I-、Cl-、F-的还原性逐渐减弱 | D. | PH3、H2S、HCl的稳定性逐渐增强 |
分析 A.金属性越强,最高价氧化物对应水合物的碱性越强;
B.非金属性越强,最高价含氧酸的酸性越强;
C.非金属性越强,对应离子的还原性越强;
D.非金属性越强,对应氢化物的稳定性越强.
解答 解:A.金属性Na>Mg>Al,最高价氧化物对应水合物的碱性强弱为:NaOH>Mg(OH)2>Al(OH)3,故A错误;
B.非金属性:Cl>Br>I,则最高价含氧酸的酸性:HClO4>HBrO4>HIO4,故B正确;
C.非金属性:I<Cl<F,则离子的还原性:I->Cl->F-,故C正确;
D.非金属性:P<S<Cl,则氢化物的稳定性:PH3<H2S<HCl,故D正确;
故选A.
点评 本题考查了原子结构与元素周期律的应用,题目难度不大,明确元素周期律的内容为解答关键,注意掌握元素周期表结构、元素周期律内容,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
11.下列物质属于酯类的是①花生油 ②柴油 ③牛油 ④机油⑤汽油 ⑥菜籽油 ⑦煤焦油( )
| A. | ②③④⑦ | B. | ①③⑥ | C. | ⑤⑥⑦ | D. | ②⑤ |
9.下列说法中不正确的是( )
| A. | 用原电池装置都能实现2HCl+Cu=CuCl2+H2↑ 反应 | |
| B. | 放热反应在常温条件下不一定能发生 | |
| C. | 1mol硫酸跟足量氢氧化钠发生中和反应放出的热叫做中和热 | |
| D. | 对于吸热反应,反应物所具有的总能量低于生成物所具有的总能量 |
16.元素符号、反应方程式、结构示意图、电子式、结构式等通常叫做化学用语.下列有关化学用语的表示方法中正确的是( )
| A. | H2O2的电子式: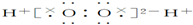 | |
| B. | NH4I的电子式: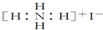 | |
| C. | 原子核内有10个中子的氧原子:1810O | |
| D. | CO2分子的结构式:O═C═O |
13.同一主族的两种元素的核外电子差值不可能为( )
| A. | 2 | B. | 8 | C. | 18 | D. | 30 |
10.将木炭与浓硫酸共热后得到的过量气体通入下列溶液中不会得到无色澄清溶液的是( )
| A. | 稀品红溶液 | B. | Ca(OH)2溶液 | C. | 溴水 | D. | 饱和H2S溶液 |
 .
.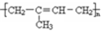 )为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.
)为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.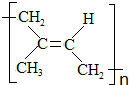 .
.