题目内容
设NA为阿伏加德罗常数的数值,则下列说法中正确的是( )
| A、80g硝酸铵含有氮原子数为2NA |
| B、标准状况下,22.4L CCl4所含分子数目为NA |
| C、常温常压下,32 g的O2和O3混合气体含有的原子数为2NA |
| D、8.4gNaHCO3溶解于水,电离生成的CO32-数目为0.1NA |
考点:阿伏加德罗常数
专题:
分析:A、根据硝酸铵的质量计算出氮原子的物质的量及数目;
B、标况下,CCl4呈液态,不能用标准状况下的气体摩尔体积计算;
C、O2和O3为同素异形体,故32g32gO2和O3含有32g氧原子;
D、HCO3-以水解为主,电离不完全,电离出的CO32-数目小于HCO3-数目.
B、标况下,CCl4呈液态,不能用标准状况下的气体摩尔体积计算;
C、O2和O3为同素异形体,故32g32gO2和O3含有32g氧原子;
D、HCO3-以水解为主,电离不完全,电离出的CO32-数目小于HCO3-数目.
解答:
解:A、80gNH4NO3的物质的量n=
=
=1mol,氮原子个数=2n?NA=2NA,故A正确;
B、标况下,CCl4呈液态,不能用标准状况下的气体摩尔体积计算,故B错误;
C、32gO2和O3含有32g氧原子,即2mol氧原子,32gO2和O3的混合气体含有2NA个氧原子,故C正确;
D、8.4gNaHCO3溶解于水电离出0.1molHCO3-,HCO3-以水解为主,不完全电离,电离生成的CO32-数目小于0.1NA,故D错误.
故选:AC.
| m |
| M |
| 80g |
| 80g/mol |
B、标况下,CCl4呈液态,不能用标准状况下的气体摩尔体积计算,故B错误;
C、32gO2和O3含有32g氧原子,即2mol氧原子,32gO2和O3的混合气体含有2NA个氧原子,故C正确;
D、8.4gNaHCO3溶解于水电离出0.1molHCO3-,HCO3-以水解为主,不完全电离,电离生成的CO32-数目小于0.1NA,故D错误.
故选:AC.
点评:本题考查了阿伏伽德罗常数,题目浓度不大,注意标准状况下物质的状态.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、在有盐桥构成的铜-锌-稀硫酸原电池中,盐桥中的阳离子移向电池的锌极 |
| B、化学平衡的建立与途径无关,可以从正反应方向建立,也可以从逆反应方向建立 |
| C、可以借助分光度计采用比色的方法测定某反应的化学反应速率 |
| D、在FeCl3与过量的KI溶液充分反应后的溶液用CCl4萃取后,往上层溶液中加入几滴KSCN溶液,溶液出现血红色,说明该化学反应存在限度 |
相同条件下,气体A与氧气的质量比为2:1,体积比为4:1,气体A的相对分子质量是( )
| A、16 | B、17 | C、44 | D、64 |
下列关于价电子排布为3s23p4的粒子描述正确的是( )
| A、该元素在周期表中的位置为第三周期第IVA族 |
| B、该元素的最高正价为+6价 |
| C、一定条件下,它可与H2生成液态化合物 |
D、其核外电子排布图为: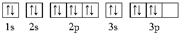 |
地壳中含量最多的元素是( )
| A、铝 | B、铁 | C、氧 | D、硅 |
下列分离或除杂方法不正确的是( )
| A、用分液法分离水和酒精 |
| B、用蒸馏法分离苯和溴苯 |
| C、用结晶法除去硝酸钾中的氯化钠杂质 |
| D、用饱和NaHCO3溶液除去CO2中混有的少量HCl气体 |
已知1g氢气在氧气中完全燃烧生成气态水,放出热量120.9kJ,则( )
| A、反应的热化学方程式:2H2(g)+O2(g)=2H2O(g)△H=+483.6 kJ?mol-1 |
| B、氢气的燃烧热为241.8 kJ?mol-1 |
| C、1 mol H2O(l)的能量大于1 mol H2O(g)的能量 |
| D、2 mol H2和1 mol O2的能量总和大于2 mol H2O(g)的能量 |
下列各组物质中,依次属于单质、酸、盐的一组是( )
| A、干冰、石灰石、氧化钙 |
| B、氧气、氢氯酸、氯化铵 |
| C、水、烧碱、食盐 |
| D、氯水、硝酸、纯碱 |