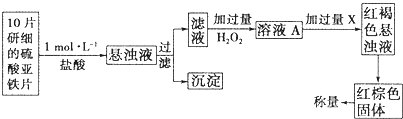
题目内容
过滤需要的仪器(或用品)有______________、______________、______________、______________、______________、______________。操作中要求做到“一贴二低三靠”,其中“二低”是_________________________________________。在蒸发操作中,注入溶液的量不要超过蒸发皿容积的______________,加热时要用玻璃棒不断搅拌溶液的原因是_________________________________________,待蒸发皿中析出较多晶体时,应停止加热的原因是_________________________________________。
铁架台 铁圈 漏斗 玻璃棒 烧杯 滤纸 滤纸上沿低于漏斗口边沿;溶液液面低于滤纸上沿 ![]() 防止局部过热,液滴飞溅 防止固体颗粒外溅,利用余热即可完全蒸发
防止局部过热,液滴飞溅 防止固体颗粒外溅,利用余热即可完全蒸发

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
 Ⅰ.下列实验操作或对实验事实的描述不正确的是
Ⅰ.下列实验操作或对实验事实的描述不正确的是