题目内容
铁是人类必需的微量元素之一,它可以促进血红蛋白结合氧分子进行输氧,医学上经常用硫酸亚铁糖衣片给患贫血的病人补铁.请根据以下药品说明书回答问题:
(1)药片上的糖衣可以起
(2)某研究小组甲欲用KMnO4测定FeSO4的含量.
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250毫升,配制时需要的仪器除托盘天平、烧杯、玻璃棒、量筒外,还需要的仪器有
②滴定时含硫酸亚铁的滤液放在
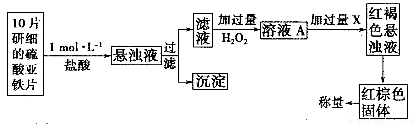
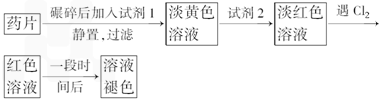
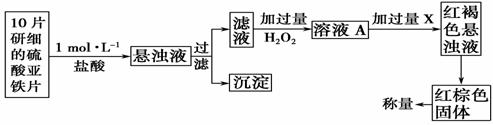
(3)另一研究小组乙设计了如下测量方案:
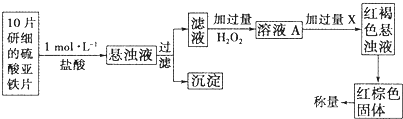
①此检验过程中加过量H2O2反应的离子方程式为
②从红褐色的悬浊液到最后的称量,其过程中所需的基本操作有
A.过滤 B.洗涤 C.萃取 D.分液 E.冷却 F.灼烧
③最后称量红棕色固体的质量为0.8960g,那么该药片中硫酸亚铁的质量分数为
分析:(1)根据亚铁离子具有强还原性和在水溶液中易发生水解作答;
(2)①根据配制一定物质的量浓度溶液实验用到的仪器回答;
②滴定实验中,待测液放在锥形瓶中,高锰酸钾溶液具有强氧化性,放在酸式滴定管中,不用加指示剂,利用高锰酸钾溶液本身的颜色即可;
(3)①H2O2与亚铁离子反应生成铁离子和水,以此写出离子方程式即可;
②从红褐色的悬浊液过滤得到含氢氧化铁的滤渣,洗涤除掉吸附的杂质离子,灼烧分解生成氧化铁,冷却后称量;
③先求出氧化铁中铁的质量,根据铁原子守恒可知硫酸亚铁的质量,然后求硫酸亚铁的质量分数即可.
(2)①根据配制一定物质的量浓度溶液实验用到的仪器回答;
②滴定实验中,待测液放在锥形瓶中,高锰酸钾溶液具有强氧化性,放在酸式滴定管中,不用加指示剂,利用高锰酸钾溶液本身的颜色即可;
(3)①H2O2与亚铁离子反应生成铁离子和水,以此写出离子方程式即可;
②从红褐色的悬浊液过滤得到含氢氧化铁的滤渣,洗涤除掉吸附的杂质离子,灼烧分解生成氧化铁,冷却后称量;
③先求出氧化铁中铁的质量,根据铁原子守恒可知硫酸亚铁的质量,然后求硫酸亚铁的质量分数即可.
解答:解:(1)亚铁离子具有强还原性,容易被空气中的氧气氧化,糖衣可以隔绝空气,防止亚铁离子被氧气氧化,亚铁离子在水溶液中易水解,加盐酸增大氢离子浓度可以抑制水解,
故答案为:隔绝空气,防止被O2氧化;防止Fe2+水解;
(2)①配制一定物质的量浓度溶液实验用到的仪器除托盘天平、烧杯、玻璃棒、量筒外,还需要250mol容量瓶和定容时使用的胶头滴管,
故答案为:250mol容量瓶;胶头滴管;
②滴定实验中,待测液放在锥形瓶中,因此含硫酸亚铁的滤液放在锥形瓶,高锰酸钾溶液具有强氧化性,放在酸式滴定管中;不用加指示剂,利用高锰酸钾溶液本身的颜色即可,当加入最后一滴酸性高锰酸钾溶液时,锥形瓶中溶液的颜色变为紫色,震荡,且半分钟内不恢复原色,则滴定到了终点,
故答案为:锥形瓶;酸式滴定管;不用加;最后一滴酸性高锰酸钾溶液时,锥形瓶中溶液的颜色变为紫色,震荡,且半分钟内不恢复原色,则滴定到了终点;
(3)①H2O2与亚铁离子反应生成铁离子和水,离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②从红褐色的悬浊液过滤得到含氢氧化铁的滤渣,洗涤除掉吸附的杂质离子,灼烧分解生成氧化铁,冷却后称量,
故答案为:A、B、F、E;
③氧化铁中铁元素的质量为:0.8960g×
=0.6272g,根据铁元素守恒可知硫酸亚铁中铁元素的质量为0.6272g,则硫酸亚铁的质量为:0.6272g×
=1.7024g,因此硫酸亚铁的质量为:
×100%=56.7%,
故答案为:56.7%.
故答案为:隔绝空气,防止被O2氧化;防止Fe2+水解;
(2)①配制一定物质的量浓度溶液实验用到的仪器除托盘天平、烧杯、玻璃棒、量筒外,还需要250mol容量瓶和定容时使用的胶头滴管,
故答案为:250mol容量瓶;胶头滴管;
②滴定实验中,待测液放在锥形瓶中,因此含硫酸亚铁的滤液放在锥形瓶,高锰酸钾溶液具有强氧化性,放在酸式滴定管中;不用加指示剂,利用高锰酸钾溶液本身的颜色即可,当加入最后一滴酸性高锰酸钾溶液时,锥形瓶中溶液的颜色变为紫色,震荡,且半分钟内不恢复原色,则滴定到了终点,
故答案为:锥形瓶;酸式滴定管;不用加;最后一滴酸性高锰酸钾溶液时,锥形瓶中溶液的颜色变为紫色,震荡,且半分钟内不恢复原色,则滴定到了终点;
(3)①H2O2与亚铁离子反应生成铁离子和水,离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②从红褐色的悬浊液过滤得到含氢氧化铁的滤渣,洗涤除掉吸附的杂质离子,灼烧分解生成氧化铁,冷却后称量,
故答案为:A、B、F、E;
③氧化铁中铁元素的质量为:0.8960g×
| 112 |
| 160 |
| 152 |
| 56 |
| 1.7024g |
| 0.3g×10 |
故答案为:56.7%.
点评:本题考查亚铁离子的性质,涉及亚铁离子的强还原性、水解反应和实验仪器的选取、实验步骤的设计和滴定终点的确定,计算硫酸亚铁质量分数根据铁元素守恒计算可减少计算工作量.

练习册系列答案
相关题目