题目内容
下列液体均处于25℃,有关叙述正确的是
- A.某物质的溶液pH<7,向该溶液中加入氢氧化钠溶液,Kw增大
- B.pH=8的NaOH溶液稀释100倍,其pH=6
- C.将1L 0.1mol·L-1的Ba(OH)2溶液稀释为2L,pH=12
- D.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍
D
试题分析:A、Kw是温度的函数,温度没变,Kw不变,错误;B、NaOH溶液稀释后尽管浓度很小,但还是显碱性的,即pH接近7但大于7,错误;C、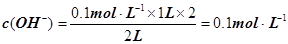 ,
,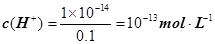 ,pH=-lgc(H+) =-lg10–13=13,错误;D、pH=4.5的番茄汁中c(H+) =10–4.5,pH=6.5的牛奶中c(H+) =10–6.5,
,pH=-lgc(H+) =-lg10–13=13,错误;D、pH=4.5的番茄汁中c(H+) =10–4.5,pH=6.5的牛奶中c(H+) =10–6.5,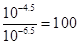 ,故D正确。
,故D正确。
考点:考查水的离子积和pH计算。
试题分析:A、Kw是温度的函数,温度没变,Kw不变,错误;B、NaOH溶液稀释后尽管浓度很小,但还是显碱性的,即pH接近7但大于7,错误;C、
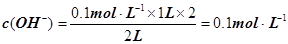 ,
,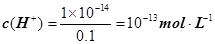 ,pH=-lgc(H+) =-lg10–13=13,错误;D、pH=4.5的番茄汁中c(H+) =10–4.5,pH=6.5的牛奶中c(H+) =10–6.5,
,pH=-lgc(H+) =-lg10–13=13,错误;D、pH=4.5的番茄汁中c(H+) =10–4.5,pH=6.5的牛奶中c(H+) =10–6.5,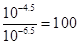 ,故D正确。
,故D正确。考点:考查水的离子积和pH计算。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列液体均处于25℃,下列有关叙述正确的是( )
| A、PH值相同的盐酸和氯化铵溶液中水的电离程度相同 | B、某溶液中由水电离出的c(H+)=10-13,则该溶液的PH一定为13 | C、PH=4.5的番茄汁中c(H+)是PH=6.5的牛奶中c(H+)的2倍 | D、中和浓度和体积均相同的盐酸和醋酸,消耗的氢氧化钠的物质的量之比为1:1 |