题目内容
9.配制490mL1.0mol•L-1的NaOH溶液,下列说法正确的是( )| A. | 需用托盘天平称取NaOH固体19.6g | |
| B. | 氢氧化钠固体溶解之后迅速转移至容量瓶中,以防变质 | |
| C. | 加蒸馏水至离刻度线1~2cm时改用胶头滴管定容 | |
| D. | 容量瓶使用前没有干燥会使所配溶液浓度偏低 |
分析 A.配制490mL1.0mol•L-1的NaOH溶液,实际应选择500mL容量瓶,依据m=CVM计算需要溶质的质量;
B.依据容量瓶使用注意事项解答;
C.依据定容的正确操作解答;
D.定容时,需要向容量瓶中加入蒸馏水,所以容量瓶使用前不需要干燥.
解答 解:A.配制490mL1.0mol•L-1的NaOH溶液,实际应选择500mL容量瓶,需要溶质的质量m=1.0mol/L×0.5L×40g/mol=20.0g,故A错误;
B.容量瓶为精密仪器,不能盛放过热液体,且只有在室温下体积才准确,所以应冷却后再移液,故B错误;
C.定容时,为防止加水过多,加蒸馏水至离刻度线1~2cm时改用胶头滴管逐滴滴加,故C正确;
D.定容时,需要向容量瓶中加入蒸馏水,所以容量瓶使用前不需要干燥,故D错误;
故选:C.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及容量瓶使用方法是解题关键,题目难度不大.

练习册系列答案
相关题目
19.下列说法中正确的是( )
| A. | 在BF3、NaCl3分子中,所有原子都满足8电子稳定机构 | |
| B. | P4和CH4空间结构相同,其具有的化学键类型也完全相同 | |
| C. | Cl-的结构示意图可表示为 | |
| D. | COS的电子式可表示为 |
20.一氧化碳、甲醛、二氧化硫均有毒,均是常见的大气污染物.
(1)人们常用催化剂来选择反应进行的方向,如图1为一定条件下1 molCH3OH与O2发生反应时,生成CO或CO2或HCHO的能量变化[反应物O2(g)和生成物H2O(g)已略去].
①在有催化剂的作用下,CH3OH与O2反应的主要产物是HCHO(填“CO”“CO2”或“HCHO”).
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g)△H=-470KJ•mol-1.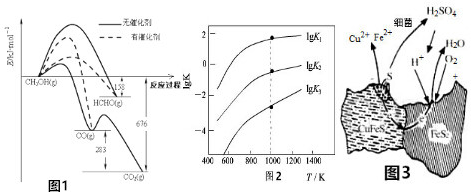
(2)煤炭中的硫主要以黄铁矿的形式存在,用氢气脱出黄铁矿中硫的相关反应见下表,其相关反应的平衡常数的对数值与温度的关系如图2.
①上述反应中,△H1>(填“>”或“<”)0.
②提高硫的脱除率可采取的措施有升高温度(任填一种).
③1000K时,向2L恒容密闭容器中充入一定量的H2(g)和FeS2(g),只发生反应①,达到平衡时,H2的转化率为99%.
(3)用细菌冶炼铜时,当黄铜矿中伴有黄铁矿时,可明显提高浸取速率,其原理如图3.
①冶炼过程中,正极周围溶液的pH增大(填“增大”“减小”或“不变”).
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.
(1)人们常用催化剂来选择反应进行的方向,如图1为一定条件下1 molCH3OH与O2发生反应时,生成CO或CO2或HCHO的能量变化[反应物O2(g)和生成物H2O(g)已略去].
①在有催化剂的作用下,CH3OH与O2反应的主要产物是HCHO(填“CO”“CO2”或“HCHO”).
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g)△H=-470KJ•mol-1.

(2)煤炭中的硫主要以黄铁矿的形式存在,用氢气脱出黄铁矿中硫的相关反应见下表,其相关反应的平衡常数的对数值与温度的关系如图2.
| 相关反应 | 反应热 | 平衡常数K |
| ①FeS2(s)+H2(g)?FeS(s)+H2S(g) | △H1 | K1 |
| ②$\frac{1}{2}$FeS2(s)+H2(g)?$\frac{1}{2}$FeS(s)+H2S(g) | △H2 | K2 |
| ③FeS(s)+H2(g)?Fe(s)+H2S(g) | △H3 | K3 |
②提高硫的脱除率可采取的措施有升高温度(任填一种).
③1000K时,向2L恒容密闭容器中充入一定量的H2(g)和FeS2(g),只发生反应①,达到平衡时,H2的转化率为99%.
(3)用细菌冶炼铜时,当黄铜矿中伴有黄铁矿时,可明显提高浸取速率,其原理如图3.
①冶炼过程中,正极周围溶液的pH增大(填“增大”“减小”或“不变”).
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.

 Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证该结论,学生设计了如图所示的实验装置进行实验(夹持装置略去).请回答下列问题:
Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证该结论,学生设计了如图所示的实验装置进行实验(夹持装置略去).请回答下列问题: HCl+HClO;2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑(用化学方程式表示)
HCl+HClO;2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑(用化学方程式表示) .
.