题目内容
19.下列有关化学用语表示正确的是( )| A. | 质子数为53、中子数为78的碘原子:${\;}_{53}^{131}$I | |
| B. | 乙醇的结构简式:C2H6O | |
| C. | S2-的结构示意图: | |
| D. | 甲烷分子的比例模型是 |
分析 A.元素符号的左上角为质量数;
B.结构简式中需要表示出含有的官能团结构;
C.S原子最外层6个电子,得到2个电子达到稳定结构;
D.比例模型能反映出分子中原子的大小比例关系.
解答 解:A.元素符号的左上角为质量数=质子数+中子数=53+78=131,${\;}_{53}^{131}$I,故A正确;
B.乙醇的结构简式:CH3CH2OH,C2H6O是分子式,故B错误;
C.S原子最外层6个电子,得到2个电子达到稳定结构,S2-的离子结构示意图: ,故C错误;
,故C错误;
D.甲烷分子的比例模型应该体现出甲烷分子中各原子的相对体积大小, 为甲烷的球棍模型,甲烷的比例模型为:
为甲烷的球棍模型,甲烷的比例模型为: ,故D错误;
,故D错误;
故选A.
点评 本题考查常用化学用语的书写,题目难度不大,掌握常用化学用语的书写,会阴阳离子中核外电子数的计算方法是解本题的关键.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
9.根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是( )
①Cl2+2KI=I2+2KCl ②2FeCl3+2HI=I2+2FeCl2+2HCl
③2FeCl2+Cl2=2FeCl3 ④I2+SO2+2H2O=2HI+H2SO4.
①Cl2+2KI=I2+2KCl ②2FeCl3+2HI=I2+2FeCl2+2HCl
③2FeCl2+Cl2=2FeCl3 ④I2+SO2+2H2O=2HI+H2SO4.
| A. | Cl2>I2>Fe3+>SO2 | B. | Fe3+>Cl2>I2>SO2 | C. | Cl2>Fe3+>I2>SO2 | D. | Cl2>Fe3+>SO2>I2 |
10.下列化学用语正确的是( )
| A. | 氯化氢的电子式: | B. | H2O的结构式:H-O-H | ||
| C. | 氯原子的结构示意图: | D. | CH4的比例模型: |
7.下列关于化学反应限度的说法中正确的是( )
| A. | 当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度 | |
| B. | 当一个可逆反应达到平衡状态时,这个反应的正向反应速率和逆向反应速率相等,反应也就停止了 | |
| C. | 平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变了 | |
| D. | 化学反应的限度不可以通过改变条件而改变 |
14.由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是( )
| 选项 | 反应类型 | 反应条件 |
| A | 加成、取代、消去 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
| B | 消去、加成、取代 | NaOH醇溶液/加热、常温、KOH水溶液/加热 |
| C | 氧化、取代、消去 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
| D | 消去、加成、水解 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
| A. | A | B. | B | C. | C | D. | D |
4.2015年,我国科学家屠呦呦因发现青蒿素而荣获诺贝尔奖.由植物黄花蒿叶中提取的青蒿素还可合成用于抗氯喹恶性疟及凶险型疟疾的蒿甲醚,器合成路线如图:

下列说法不正确的是( )

下列说法不正确的是( )
| A. | 青蒿素的分子式是C15H22O5,属于烃的衍生物 | |
| B. | 双氢青蒿素中含有过氧键,遇湿润的淀粉碘化钾试纸立刻显蓝色 | |
| C. | 蒿甲醚可以发生水解反应 | |
| D. | 反应②为取代反应,有H2O生成 |
11.下列化学用语表达正确的是( )
| A. | 氟离子的结构示意图: | B. | 甲烷分子的球棍模型: | ||
| C. | NaCl的电子式: | D. | 乙烯的结构简式:C2H4 |
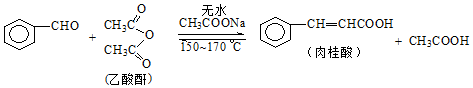
2. 肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
药品物理常数
空气冷凝管温度计
Ⅰ合成:反应装置如图所示.向三颈烧瓶中先后加入研细的无水醋酸钠、5.3g苯甲醛和6.1g乙酸酐,振荡使之混合均匀.在150~170℃加热1小时,保持微沸状态.
(1)空气冷凝管的作用是使反应物冷凝回流.
(2)该装置的加热方法是空气浴(或油浴);不能用醋酸钠晶体(CH3COONa•3H2O)的原因是乙酸酐遇热水水解;.
(3)加热回流要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是乙酸酐蒸出,反应物减少,平衡左移.
Ⅱ粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
反应混合物加入饱和碳酸钠溶液蒸馏除去苯甲醛盐酸酸化操作I过滤、洗涤干燥肉桂酸晶体
(4)加饱和Na2CO3溶液除了转化醋酸,主要目的是将肉桂酸转化为肉桂酸钠,溶解于水.
(5)操作I是加热浓缩、冷却结晶;若所得肉桂酸晶体中仍然有杂质,欲提高纯度可以进行的操作是重结晶(均填操作名称).
(6)若最后得到纯净的肉桂酸5.0g,则该反应中的产率是67.6%(保留三位有效数字).
 肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
药品物理常数
| 苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
| 溶解度(25℃,g/100g水) | 0.3 | 遇热水水解 | 0.04 | 互溶 |
| 沸点(℃) | 179.6 | 138.6 | 300 | 118 |
Ⅰ合成:反应装置如图所示.向三颈烧瓶中先后加入研细的无水醋酸钠、5.3g苯甲醛和6.1g乙酸酐,振荡使之混合均匀.在150~170℃加热1小时,保持微沸状态.
(1)空气冷凝管的作用是使反应物冷凝回流.
(2)该装置的加热方法是空气浴(或油浴);不能用醋酸钠晶体(CH3COONa•3H2O)的原因是乙酸酐遇热水水解;.
(3)加热回流要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是乙酸酐蒸出,反应物减少,平衡左移.
Ⅱ粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:

反应混合物加入饱和碳酸钠溶液蒸馏除去苯甲醛盐酸酸化操作I过滤、洗涤干燥肉桂酸晶体
(4)加饱和Na2CO3溶液除了转化醋酸,主要目的是将肉桂酸转化为肉桂酸钠,溶解于水.
(5)操作I是加热浓缩、冷却结晶;若所得肉桂酸晶体中仍然有杂质,欲提高纯度可以进行的操作是重结晶(均填操作名称).
(6)若最后得到纯净的肉桂酸5.0g,则该反应中的产率是67.6%(保留三位有效数字).